题目内容
9.下列物质的转化在给定条件下能实现的是( )| A. | S$\stackrel{O_{2}点燃}{→}$ SO3$\stackrel{足量氨水}{→}$(NH4)2SO4 | |
| B. | NH3$→_{加热}^{O_{2}/催化剂}$NO$\stackrel{O_{2}}{→}$ NO2 | |
| C. | Fe$→_{加热}^{少量Cl_{2}}$ FeCl2$→_{溶液}^{NaOH溶液}$Fe(OH)2 | |
| D. | Al$→_{溶液}^{NaOH溶液}$ NaAlO2$\stackrel{足量盐酸}{→}$Al(OH)3 |
分析 A、硫燃烧生成二氧化硫;
B、氨气催化氧化生成一氧化氮,一氧化氮氧化生成二氧化氮;
C、铁与氯气反应生成氯化铁;
D、偏铝酸钠与过量的盐酸反应生成氯化钠和氯化铝.
解答 解:A、硫燃烧生成二氧化硫,不能生成三氧化硫,故A错误;
B、氨气催化氧化生成一氧化氮,一氧化氮氧化生成二氧化氮,可以实现各步转化,故B正确;
C、铁与氯气反应生成氯化铁,而不是氯化亚铁,故C错误;
D、偏铝酸钠与过量的盐酸反应生成氯化钠和氯化铝,不生成氢氧化铝,故D错误;
故选B.
点评 本题考查化合物的性质,题目难度不大,熟练掌握物质的性质是解决此类问题的关键,正确运用物质分类及反应规律则是解决此类问题的有效方法.

练习册系列答案
相关题目
19.实验室用粗锌(含铅等杂质)与过量的稀硫酸反应制氢气的废液制备硫酸锌晶体,其流程如图1:

已知ZnSO4的溶解度如表所示:
(1)实验过程中多次用到如图2所示的过滤装置,仪器a的名称为抽滤瓶.
(2)滤渣Ⅰ的主要成分为PbSO4.X的化学式为ZnO或Zn(OH)2.
(3)溶解过程中加入的稀硫酸的作用是制备ZnSO4并抑制ZnSO4水解.
(4)结晶的操作为蒸发浓缩、冷却结晶.
(5)用酒精进行洗涤的原因是减少硫酸锌晶体的损失,容易干燥.

已知ZnSO4的溶解度如表所示:
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 60 | 80 | 100 |
| 溶解度/g | 41.6 | 47.5 | 53.8 | 61.3 | 70.5 | 75.4 | 71.1 | 60.5 |
(2)滤渣Ⅰ的主要成分为PbSO4.X的化学式为ZnO或Zn(OH)2.
(3)溶解过程中加入的稀硫酸的作用是制备ZnSO4并抑制ZnSO4水解.
(4)结晶的操作为蒸发浓缩、冷却结晶.
(5)用酒精进行洗涤的原因是减少硫酸锌晶体的损失,容易干燥.
20.下列各组离子因发生氧化还原反应而不能大量共存的是( )
| A. | H+、Fe2+、NO3-、SO42- | B. | Al3+、Na+、SO42-、HCO3- | ||
| C. | Na+、Ca2+、Cl-、SO42- | D. | Fe3+、K+、SCN-、Cl- |
17.NA表示阿伏加德罗常数的数值,下列判断正确的是 ( )
| A. | 25℃,pH=13的NaOH溶液中含有OH-的数目为0.1NA | |
| B. | 常温常压下,22.4LCO2中含有的CO2分子数为NA个 | |
| C. | 等物质的量的N2和CO的质量均为28g | |
| D. | 常温下,1L 0.1mol/LNa2CO3溶液中,含有阴离子的总数大于0.1NA |
4.如图是某化学反应过程中能量变化的曲线图.下列有关叙述正确的是( )


| A. | 该反应为吸热反应 | |
| B. | 该图可以表示Ba(OH)2•8H2O与NH4Cl的反应 | |
| C. | 化学反应中的能量变化只表现为热量的变化 | |
| D. | 化学反应中有旧键断裂就一定有新键形成 |
14.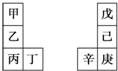 甲~辛等元素在周期表中的相对位置如右表.甲与戊的原子序数相差3,戊的一种单质是自然界硬度最大的物质,丁与辛属同周期元素,下列判断正确的是( )
甲~辛等元素在周期表中的相对位置如右表.甲与戊的原子序数相差3,戊的一种单质是自然界硬度最大的物质,丁与辛属同周期元素,下列判断正确的是( )
 甲~辛等元素在周期表中的相对位置如右表.甲与戊的原子序数相差3,戊的一种单质是自然界硬度最大的物质,丁与辛属同周期元素,下列判断正确的是( )
甲~辛等元素在周期表中的相对位置如右表.甲与戊的原子序数相差3,戊的一种单质是自然界硬度最大的物质,丁与辛属同周期元素,下列判断正确的是( )| A. | 金属性:甲>乙>丁 | |
| B. | 最高价氧化物水化物酸性:戊<己 | |
| C. | 丙与庚的原子核外电子数相差13 | |
| D. | 乙的单质在空气中燃烧生成只含离子键的化合物 |
18.标准状况下,1体积水可溶解448体积的HCl 气体,制得的盐酸溶液密度为1.2g•mL-1,所得溶液的物质的量浓度为( )
| A. | 1.16 mol•L-1 | B. | 6.8 mol•L-1 | C. | 13.9 mol•L-1 | D. | 20.0 mol•L-1 |
19.有机物分子中原子间或基团间的相互影响会导致同一原子或基团的化学性质出现差异.下列事实不能说明上述观点的是( )
| A. | 苯酚能与氢氧化钠溶液反应,乙醇不能与氢氧化钠溶液反应 | |
| B. | 甲烷不能使使酸性KMnO4溶液褪色,甲苯能使使酸性KMnO4溶液褪色 | |
| C. | 苯与硝酸在50-60℃发生取代反应,甲苯与硝酸在30℃就能发生取代反应 | |
| D. | 苯能发生加成反应,环己烷不能发生加成反应 |