题目内容
17.NA表示阿伏加德罗常数的数值,下列判断正确的是 ( )| A. | 25℃,pH=13的NaOH溶液中含有OH-的数目为0.1NA | |
| B. | 常温常压下,22.4LCO2中含有的CO2分子数为NA个 | |
| C. | 等物质的量的N2和CO的质量均为28g | |
| D. | 常温下,1L 0.1mol/LNa2CO3溶液中,含有阴离子的总数大于0.1NA |
分析 A、溶液体积不明确;
B、常温常压下,气体摩尔体积大于22.4L/mol;
C、氮气和CO的物质的量不明确;
D、碳酸根水解会导致阴离子个数增多.
解答 解:A、溶液体积不明确,故溶液中含有的氢氧根的个数无法计算,故A错误;
B、常温常压下,气体摩尔体积大于22.4L/mol,故22.4L二氧化碳的物质的量小于1mol,则含有的分子个数小于NA个,故B错误;
C、等物质的量的氮气和CO的质量相同,但不一定是1mol,故质量不一定为28g,故C错误;
D、碳酸根水解会导致阴离子个数增多:CO32-+H2O?HCO3-+OH-,故溶液中的阴离子的个数多于0.1NA个,故D正确.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案
相关题目
7.相对分子质量为100的饱和链状烷烃,同分异构体中主链有5个原子的有( )
| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
12.如表列出了前20号元素中的某些元素性质的一些数据:
(1)以上10种元素中,电负性最大的是O(填元素符号).
(2)写出下列有关反应的化学方程式:
①E的单质与I元素的最高价氧化物对应的水化物反应:C+4HNO3(浓)=CO2↑+4NO2↑+2H2O.
②B2C2与EC2反应:2K2O2+2CO2=2K2CO3+O2.
(3)A元素原子核外电子排布图是1s22s22p63s23p4;比元素B原子序数大11的元素的原子的电子排布式是1s22s22p63s23p63d104s2或者[Ar]3d104s2.
(4)C和I相比较,非金属性较弱的是氮(填元素名称).
| 元素 性质 | A | B | C | D | E | F | G | H | I | J |
| 原子半径(10-10 m) | 1.02 | 2.27 | 0.74 | 1.43 | 0.77 | 1.10 | 0.99 | 1.86 | 0.75 | 1.17 |
| 最高 价态 | +6 | +1 | - | +3 | +4 | +5 | +7 | +1 | +5 | +4 |
| 最低 价态 | -2 | - | -2 | - | -4 | -3 | -1 | - | -3 | -4 |
(2)写出下列有关反应的化学方程式:
①E的单质与I元素的最高价氧化物对应的水化物反应:C+4HNO3(浓)=CO2↑+4NO2↑+2H2O.
②B2C2与EC2反应:2K2O2+2CO2=2K2CO3+O2.
(3)A元素原子核外电子排布图是1s22s22p63s23p4;比元素B原子序数大11的元素的原子的电子排布式是1s22s22p63s23p63d104s2或者[Ar]3d104s2.
(4)C和I相比较,非金属性较弱的是氮(填元素名称).
9.下列物质的转化在给定条件下能实现的是( )
| A. | S$\stackrel{O_{2}点燃}{→}$ SO3$\stackrel{足量氨水}{→}$(NH4)2SO4 | |
| B. | NH3$→_{加热}^{O_{2}/催化剂}$NO$\stackrel{O_{2}}{→}$ NO2 | |
| C. | Fe$→_{加热}^{少量Cl_{2}}$ FeCl2$→_{溶液}^{NaOH溶液}$Fe(OH)2 | |
| D. | Al$→_{溶液}^{NaOH溶液}$ NaAlO2$\stackrel{足量盐酸}{→}$Al(OH)3 |
6.关于下列装置的说法中,不正确的是( )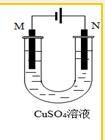

| A. | 若用于精炼粗铜,所得电解铜的纯度可达99.95%~99.98% | |
| B. | 若用于精炼粗铜,在N极附近得到阳极泥,可作为提炼金、银等贵重金属的原料 | |
| C. | 若用于精炼粗铜,则M极为粗铜 | |
| D. | 若用于铁片镀铜,则M极为铁片 |
7.下列物质属于天然纤维且其主要成分是纤维素的是( )
| A. | 棉花 | B. | 光导纤维 | C. | 人造棉 | D. | 蚕丝 |
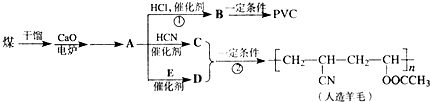
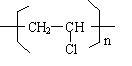 ,CH2C═CH-CN.
,CH2C═CH-CN.