题目内容
 为了研究外界条件对过氧化氢分解速率的影响,某同学做了以下实验:
为了研究外界条件对过氧化氢分解速率的影响,某同学做了以下实验:| 编号 | 操作 | 实验现象 |
| ① | 分别在试管A、B中加入5mL 5% H2O2溶液,各滴入2滴1mol?L-1 FeCl3溶液.待试管中均有适量气泡出现时,将试管A放入盛有5℃左右冷水的烧杯中浸泡;将试管B放入盛有40℃左右热水的烧杯中浸泡 | 试管A中无明显气泡产生; 试管B中产生的气泡量增加 |
| ② | 另取两支试管分别加入5mL 5% H2O2溶液和 5mL 10% H2O2溶液 | 试管A、B中均未明显见到有气泡产生 |
(1)过氧化氢分解的化学方程式为
(2)实验①的目的是
(3)实验②未观察到预期的实验现象.为了帮助该同学达到实验目的,你提出的对上述操作的改进意见是
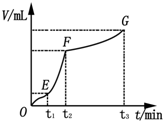
(4)某同学在50mL一定浓度的H2O2溶液中加入一定量的二氧化锰,放出气体的体积(标准状况下)与反应时间的关系如图所示,分析判断OE、EF、FG三段中,
考点:探究影响化学反应速率的因素
专题:实验设计题
分析:(1)过氧化氢分解生成氧气和水;
(2)根据试管A、B实验操作的异同点解答;
(3)根据影响化学反应速率的外界因素解答;
(4)根据速率的表示方法和图象横坐标和纵坐标的意义解答.
(2)根据试管A、B实验操作的异同点解答;
(3)根据影响化学反应速率的外界因素解答;
(4)根据速率的表示方法和图象横坐标和纵坐标的意义解答.
解答:
解:(1)过氧化氢分解,FeCl3在此反应中作催化剂,起催化作用,能加快过氧化氢分解产生氧气的速率,故答案为:2H2O2
2H2O+O2↑;
(2)分别在试管A、B中加入 5mL 5% H2O2溶液,各滴入1~2 滴1mol/L 溶液.待试管中均有适量气泡出现,说明过氧化氢分解能发生,试管A、B中均有适量气泡出现时,将试管A放入盛有5℃左右冷水的烧杯中;将试管B放入盛有40℃左右热水的烧杯中,两支试管不同点是试管A的温度比试管B的温度低,说明研究的是温度对反应速率的影响,而开始加滴加FeCl3溶液,目的加快H2O2分解,
故答案为:研究温度对H2O2分解速率的影响;作为催化剂,加快H2O2分解速率;
(3)影响化学反应速率的外界因素有浓度、温度、气体的压强、催化剂、固体的表面积,另取两支试管分别加入 5mL 5%H2O2溶液和 5mL10%H2O2溶液,试管A、B中均未见气泡产生,为加快反应速率,可从温度、或催化剂的影响角度考虑,
故答案为:将两支试管同时放入盛有相同温度热水的烧杯中,或向两支试管中同时滴入2滴1mol/L FeCl3溶液,观察产生气泡的速率;
(4)该图象横坐标表示时间,纵坐标表示生成气体的体积,时间越短生成的气体越多,反应速率越快,所以速率最快的为EF,故答案为:EF.
| ||
(2)分别在试管A、B中加入 5mL 5% H2O2溶液,各滴入1~2 滴1mol/L 溶液.待试管中均有适量气泡出现,说明过氧化氢分解能发生,试管A、B中均有适量气泡出现时,将试管A放入盛有5℃左右冷水的烧杯中;将试管B放入盛有40℃左右热水的烧杯中,两支试管不同点是试管A的温度比试管B的温度低,说明研究的是温度对反应速率的影响,而开始加滴加FeCl3溶液,目的加快H2O2分解,
故答案为:研究温度对H2O2分解速率的影响;作为催化剂,加快H2O2分解速率;
(3)影响化学反应速率的外界因素有浓度、温度、气体的压强、催化剂、固体的表面积,另取两支试管分别加入 5mL 5%H2O2溶液和 5mL10%H2O2溶液,试管A、B中均未见气泡产生,为加快反应速率,可从温度、或催化剂的影响角度考虑,
故答案为:将两支试管同时放入盛有相同温度热水的烧杯中,或向两支试管中同时滴入2滴1mol/L FeCl3溶液,观察产生气泡的速率;
(4)该图象横坐标表示时间,纵坐标表示生成气体的体积,时间越短生成的气体越多,反应速率越快,所以速率最快的为EF,故答案为:EF.
点评:本题主要考查学生的实验探究能力,解答时须注意实验的原理,难度中等.

练习册系列答案
相关题目
下列叙述Ⅰ和Ⅱ均正确并且有因果关系的是( )
| 选项 | 叙述Ⅰ | 叙述Ⅱ |
| A | 晶体硅熔点高硬度大 | 可用于制作半导体材料 |
| B | 氢氧化铝具有弱碱性 | 可用于制胃酸中和剂 |
| C | 漂白粉在空气中不稳定 | 可用于漂白纸张 |
| D | 氧化铁能与酸反应 | 可用于制作红色涂料 |
| A、A | B、B | C、C | D、D |
下列说法正确的是( )
| A、同温同压下甲烷和氧气的密度之比2:1 |
| B、1g甲烷和1g 氧气的原子数之比为5:1 |
| C、等物质的量的甲烷和氧气的质量之比2:1 |
| D、等质量的甲烷和氧气的体积之比为2:1 |
 (1)有A、B、C、D四种金属,已知:只有D投入水中可与水剧烈反应;用B和C作电极,稀硫酸作电解质溶液构成原电池时,C为正极;A和C的离子共存于电解液中,以石墨为电极电解时阴极析出A.则这四种金属的活动性由强到弱的顺序是
(1)有A、B、C、D四种金属,已知:只有D投入水中可与水剧烈反应;用B和C作电极,稀硫酸作电解质溶液构成原电池时,C为正极;A和C的离子共存于电解液中,以石墨为电极电解时阴极析出A.则这四种金属的活动性由强到弱的顺序是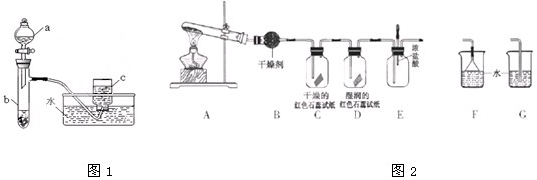
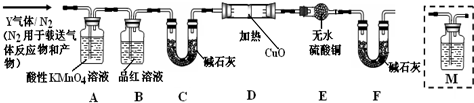
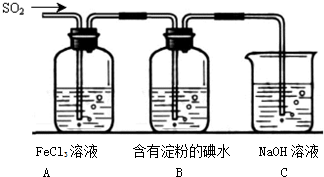
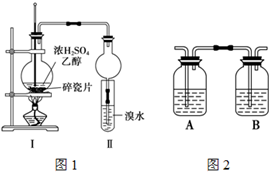 某化学兴趣小组用如图1所示装置进行探究实验,以验证产物中有乙烯生成且乙烯具有不饱和性.当温度迅速上升后,可观察到试管中溴水褪色,烧瓶中浓H2SO4与乙醇的混合液体变为棕黑色.
某化学兴趣小组用如图1所示装置进行探究实验,以验证产物中有乙烯生成且乙烯具有不饱和性.当温度迅速上升后,可观察到试管中溴水褪色,烧瓶中浓H2SO4与乙醇的混合液体变为棕黑色.