题目内容
下列说法正确的是( )
| A、同温同压下甲烷和氧气的密度之比2:1 |
| B、1g甲烷和1g 氧气的原子数之比为5:1 |
| C、等物质的量的甲烷和氧气的质量之比2:1 |
| D、等质量的甲烷和氧气的体积之比为2:1 |
考点:阿伏加德罗定律及推论
专题:
分析:A.同温同压下,气体摩尔体积相等,根据ρ=
计算其密度之比;
B.根据N=
NA计算其分子个数之比,再结合分子构成计算原子个数之比;
C.根据m=nM计算其质量之比;
D.根据V=
Vm计算其体积之比.
| M |
| Vm |
B.根据N=
| m |
| M |
C.根据m=nM计算其质量之比;
D.根据V=
| m |
| M |
解答:
解:A.同温同压下,气体摩尔体积相等,根据ρ=
知,二者密度之比等于其摩尔质量之比=16g/mol:32g/mol=1:2,故A错误;
B.根据N=
NA知,相同质量时,二者的分子个数之比等于其摩尔质量的反比=32g/mol:16g/mol=2:1,甲烷分子中含有5个原子、氧气分子中含有2个原子,所以其原子个数之比为5:1,故B正确;
C.根据m=nM知,等物质的量的甲烷和氧气,其质量之比等于其摩尔质量之比=16g/mol:32g/mol=1:2,故C错误;
D.根据V=
Vm知,温度和压强未知,无法确定气体摩尔体积,所以无法计算其体积大小,故D错误;
故选B.
| M |
| Vm |
B.根据N=
| m |
| M |
C.根据m=nM知,等物质的量的甲烷和氧气,其质量之比等于其摩尔质量之比=16g/mol:32g/mol=1:2,故C错误;
D.根据V=
| m |
| M |
故选B.
点评:本题考查阿伏伽德罗定律及其推论,明确物质的量有关公式中各个物理量的关系是解本题关键,注意气体摩尔体积的适用范围及适用条件,为易错点.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列有关金属的说法正确的是( )
| A、生铁与钢的区别在于生铁含碳杂质,而钢不含 |
| B、铜在自然界中的含量高,所以铜是人类最早使用的金属 |
| C、黑色金属材料包括铁、铬、锰及其化合物 |
| D、金属一般都具有导电性、导热性、延展性 |
物质的量浓度相同的下列溶液,pH由小到大顺序排列的是( )
| A、(NH4)2SO4,NH4Cl,NaNO3,Na2S |
| B、Na2CO3,NaHCO3,NH4Cl,NaCl |
| C、Na2CO3,NaHCO3,NaCl,NH4Cl |
| D、NH4Cl,(NH4)2SO4,Na2S,NaNO3 |
下列关于化学用语的表示正确的是( )
A、过氧化钠的电子式: | ||
B、质子数为35、中子数为45的溴原子:
| ||
C、硫离子的结构示意图: | ||
| D、乙烯的结构简式:CH2CH2 |
同温同压下,等质量的下列各组气体含有相同数目的原子数的是( )
| A、O2与O3 |
| B、SO2与SO3 |
| C、CO2与CO |
| D、CO与N2 |
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A、0.1mol?L-1的Na2CO3溶液中,阴离子的总数目大于0.1NA |
| B、常温下,46 g NO2和N2O4混合气体中含有的分子总数为2NA |
| C、标准状况下,22.4L的HF含有NA个分子 |
| D、标准状况下,10g的庚烷分子中含有2.2NA个共价键 |
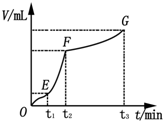 为了研究外界条件对过氧化氢分解速率的影响,某同学做了以下实验:
为了研究外界条件对过氧化氢分解速率的影响,某同学做了以下实验: