题目内容
12. 某化工厂设计要求为:空气中二氧化硫含量不得超过0.02mg/L.
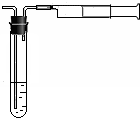
某化工厂设计要求为:空气中二氧化硫含量不得超过0.02mg/L.某同学拟用如图所示简易装置测定空气中的SO2含量:准确移取10mL5×10-4mol/L的标准碘水溶液,注入如图所示试管中,加2~3滴淀粉指示剂,此时溶液呈蓝色.在指定的测定地点抽气,每次抽气100mL,直到溶液的蓝色全部褪尽为止.假设该同学的测量是准确的,则他抽气的次数至少大于160次时方可说明该厂空气中的SO2含量达标.
分析 二氧化硫用碘溶液来吸收,方程式为:SO2+I2+2H2O═2HI+H2SO4,结合反应的方程式计算.
解答 解:二氧化硫用碘溶液来吸收,方程式为:SO2+I2+2H2O═2HI+H2SO4,为说明该地空气中的SO2含量符合排放标准,
设至少抽气x次,则抽气x次SO2的质量为100x×10-3L×2×10-5 g•L-1=(2x×10-6)g,则根据化学方程式可得出结论.
SO2~~~~~~~~~~~I2
64 g 1 mol
2x×10-6 g 10×10-3 L×5×10-4 mol•L-1
x=160,
故答案为:160.
点评 本题考查物质含量的测定,为高频考点,把握发生的化学反应为解答的关键,注意利用关系式计算简化计算,题目难度不大.

练习册系列答案
相关题目
3.可用来鉴别己烯、四氯化碳、苯的方法是( )
| A. | 酸性高锰酸钾 | B. | 溴水 | C. | 液溴 | D. | 硝化反应 |
17.按系统命名,有机物CH3CH(C2H5)CH(CH3)2的名称是( )
| A. | 1,3-二甲基戊烷 | B. | 2-甲基-3-乙基丁烷 | ||
| C. | 3,4-二甲基戊烷 | D. | 2,3-二甲基戊烷 |
2.下列离子方程式正确的是( )
| A. | 氨水吸收足量的SO2气体:OH-+SO2═HSO3- | |
| B. | 稀硝酸中加入过量铁粉:Fe+4H++NO3-═Fe3++NO↑+2H2O | |
| C. | 用NaOH溶液吸收废气中氮氧化物:NO+NO2+OH-═NO2-+H2O | |
| D. | 往AlCl3溶液中滴加过量的NaOH溶液:Al3++4OH-═AlO2-+2H2O |
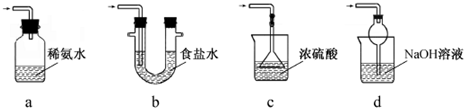





 的名称为2-氯丁烷;
的名称为2-氯丁烷; 的醇是
的醇是 (写结构简式).
(写结构简式).