题目内容
4.下列说法正确的是( )| A. | 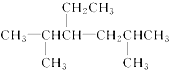 的正确名称是2,5-二甲基-4-乙基己烷 的正确名称是2,5-二甲基-4-乙基己烷 | |
| B. | 胡椒酚的结构简式为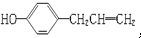 胡椒酚在水中的溶解度小于苯酚在水中的溶解度 胡椒酚在水中的溶解度小于苯酚在水中的溶解度 | |
| C. | 某有机物燃烧只生成CO2和H2O,且二者物质的量相等,则此有机物的组成为CnH2n | |
| D. | 2013年11月出现的“夺命快递”--化学品为氟乙酸甲酯,它是一种无色透明液体,不溶于水,易溶于乙醇、乙醚,属于酯类,也属于卤代烃 |
分析 A.取代基的位次和不是最小;
B.胡椒酚-OH的对位上的基团为憎水基;
C.可能含有氧元素;
D.氟乙酸甲酯中含有氧原子,属于酯类,不属于卤代烃.
解答 解:A.取代基的位次和不是最小,名称为2,5-二甲基-3-乙基己烷,故A错误;
B.胡椒酚-OH的对位上的基团为憎水基,所以胡椒酚在水中的溶解度比苯酚小,故B正确;
C.无法确定是否含有氧元素,故C错误;
D.氟乙酸甲酯属于酯类,酯类一般不溶于水,易溶于有机溶剂,由于其分子中除了含有碳氢元素外,还含有氧元素,不属于卤代烃,故D错误.
故选B.
点评 本题考查有机物的命名以及结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重酚、有机物的命名的考查,题目难度不大.

练习册系列答案
相关题目
13.在常温常压下,将10mL某气态烃充分燃烧,消耗65mL的氧气,对该烃的下列说法中正确的是( )
| A. | 该烃能使溴水褪色 | B. | 该烃有三种不同的物质 | ||
| C. | 该烃的一氯取代物4种 | D. | 该烃的二氯取代物6种 |
15.下列各组物质气化或熔化时,所克服的微粒间的作用(力),属同种类型的是( )
| A. | 碘和干冰的升华 | B. | 二氧化硅和生石灰的熔化 | ||
| C. | 氯化钠和铁的熔化 | D. | 干冰和氯化铵变成气体 |
12.NA代表阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 60g乙酸与足量乙醇发生酯化反应.充分反应后断裂的C-O键数目为NA | |
| B. | 室温下向1LpH=1的醋酸溶液中加水,所得溶液的H+数目大于0.1NA | |
| C. | 某无水乙醇与足量金属钠反应生成5.6LH2,该乙醇分子中共价键总数为4NA | |
| D. | 己知C2H4(g)+H2(g)=C2H4(g)△H=-137.0kJ/mol,乙烯与H2加成时放出68.5kJ热量,则反应过程中被破坏的碳原子之间共用电子对数目为NA |
19.科学家发现了一种新元素的原子核内有161个中子,质量数为272,该元素的核电荷数为( )
| A. | 111 | B. | 161 | C. | 272 | D. | 433 |
9.两种微粒的质子数和电子数都相等,它们不可能是( )
| A. | 一种阳离子和一种阴离子 | B. | 一种单质分子和一种化合物分子 | ||
| C. | 两种原子 | D. | 一种原子和一种分子 |
16.根据①~⑩元素的编号所在周期表中的位置,用相应的元素符号回答有关问题:
(1)能显+1价,还能显-1价的元素是H、Cl.
(2)单质具有半导体性质的元素是Si.
(3)其单质能和冷水剧烈反应的元素是Na、F.
(4)a元素能以正化合价与b元素形成AB型化合物,该化合物常温下为固态且难溶于水,则a元素是Mg,b元素是O.
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 1 | ① | ② | ||||||
| 2 | ③ | ④ | ⑤ | ⑥ | ⑦ | |||
| 3 | ⑧ | ⑨ | ⑩ |
(2)单质具有半导体性质的元素是Si.
(3)其单质能和冷水剧烈反应的元素是Na、F.
(4)a元素能以正化合价与b元素形成AB型化合物,该化合物常温下为固态且难溶于水,则a元素是Mg,b元素是O.
13.下列离子能大量共在的是( )
| A. | Ba2+、Na+、OH-、SO42- | B. | H+、Na+、I-、Cl- | ||
| C. | HCO3-、K+、NO3-、OH- | D. | H+、Fe2+、SO42-、NO3- |
14.下列解释亊实的离子方程式不正碥的是( )
| A. | 用Na2S去除废水中的Hg2+,Hg2++S2-═HgS↓ | |
| B. | 向Fe(NO3)2溶液中滴人稀硫酸.溶液由浅绿色变为黄色3Fe2++4H++NO3-=3Fe2++NO↑+2H2O | |
| C. | 用醋酸、淀粉碘化钾试纸检测加碘食盐中是否有KIO3,IO3-+6I-+6H+=3I2+3H2O | |
| D. | 消毒液的主要成分为NaClO溶液,与洁厨灵混用.产生有毐Cl2,2H+++Cl-+ClO-=Cl2↑+H2O |