题目内容
15.下列各组物质气化或熔化时,所克服的微粒间的作用(力),属同种类型的是( )| A. | 碘和干冰的升华 | B. | 二氧化硅和生石灰的熔化 | ||
| C. | 氯化钠和铁的熔化 | D. | 干冰和氯化铵变成气体 |
分析 汽化或熔化时,一般分子晶体克服分子间作用力,原子晶体克服共价键;离子晶体克服离子键;金属晶体克服金属键,先判断晶体类型,只要晶体类型相同,其微粒间的作用力就相同,所以只要晶体类型相同即可,以此来解答.
解答 解:A.碘和干冰都属分子晶体,气化时都克服分子间作用力,故A正确;
B.SiO2是原子晶体,CaO是离子晶体,熔化时克服的作用力不同,故B错误;
C.氯化钠是离子晶体,铁是金属晶体,熔化时克服的作用力不同,故C错误;
D.干冰属分子晶体克服的是分子间作用力和氯化铵是离子晶体克服的是离子键和共价键,故D错误.
故选A.
点评 本题以微粒间作用力为载体考查晶体类型,侧重考查学生对这几种晶体类型的判断能力,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
4.将两个铂电极插入KOH溶液中,向两极分别通入CH4和O2即可构成甲烷燃料电池.已知电池的总反应为CH4+2O2+2OH-=CO32-+3H2O,下列叙述正确的是( )
| A. | 通入甲烷的一极为正极,该极c(OH-)减小 | |
| B. | 通入甲烷的一极的电极反应为CH4-8e-+3H2O=CO32-+10H+ | |
| C. | 通入氧气一极发生还原反应,电极反应为O2+2H2O+4e-=4OH- | |
| D. | 该电池工作时,溶液中的阴离子向正极移动 |
6.下列物质肯定是纯净物的是( )
| A. | 汽油 | B. | 化学式为C2H6O的物质 | ||
| C. | 聚乙烯 | D. | 化学式为CH2Cl2的物质 |
7.下列说法不合理的是( )
| A. | 用分液的方法分离植物油和水的混合物 | |
| B. | 乙烷中含有少量乙烯,提纯乙烷,用酸性高锰酸钾溶液洗气 | |
| C. | 用热的纯碱(Na2CO3)溶液洗涤餐具上的油污 | |
| D. | 粗铜精炼时,粗铜做电解池的阳极,纯铜做阴极 |
4.下列说法正确的是( )
| A. | 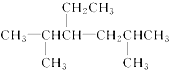 的正确名称是2,5-二甲基-4-乙基己烷 的正确名称是2,5-二甲基-4-乙基己烷 | |
| B. | 胡椒酚的结构简式为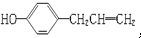 胡椒酚在水中的溶解度小于苯酚在水中的溶解度 胡椒酚在水中的溶解度小于苯酚在水中的溶解度 | |
| C. | 某有机物燃烧只生成CO2和H2O,且二者物质的量相等,则此有机物的组成为CnH2n | |
| D. | 2013年11月出现的“夺命快递”--化学品为氟乙酸甲酯,它是一种无色透明液体,不溶于水,易溶于乙醇、乙醚,属于酯类,也属于卤代烃 |
5.若溶液中由水电离产生的c(OH-)=1×10-14 mol•L-1,满足此条件的溶液中一定可以大量共存的离子组是( )
| A. | Al3+ Na+ NO3- Cl- | B. | K+ Na+ Cl- NO3- | ||
| C. | K+ Na+ Cl- CO32- | D. | K+ NH4+ SO42- NO3- |

 C6H14
C6H14 C5H10
C5H10 C7H12
C7H12 C10H8.
C10H8.