题目内容
14.已知2RCH2CHO$→_{△}^{NaOH/H_{2}O}$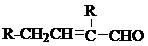
水杨酸酯E为紫外线吸收剂,可用于配制防晒霜.E的一种合成路线如图:
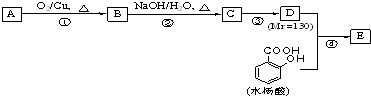
请回答下列问题:
(1)一元醇A中氧的质量分数约为21.6%,则A的分子式为C4H10O;结构分析显示A只有一个甲基,A的结构简式为1-丁醇(或正丁醇).
(2)B能与新制的Cu(OH)2发生反应,该反应的化学方程式为CH3CH2CH2CHO+2Cu(OH)2+NaOH$\stackrel{△}{→}$CH3CH2CH2COONa+Cu2O↓+3H2O.若一次取样,检验C中所含官能团,按使用的先后顺序写出所用试剂:银氨溶液、稀盐酸、溴水.
(3)第③步的反应类型为还原反应(或加成反应);D所含官能团的名称为羟基.
(4)写出同时符合下列条件的水杨酸的同分异构体的结构简式(写两个):HOCH2C≡C-C≡CCH2COOH、
 、HOCH2CH2C≡C-C≡C-COOH、
、HOCH2CH2C≡C-C≡C-COOH、 (其中两种).
(其中两种).a.分子中有6个碳原子在一条直线上;
b.分子中所含官能团包括水杨酸具有的含氧官能团.
(5)第④步的反应条件为浓H2SO4、加热;写出E的结构简式:
 .
.
分析 一元醇A中氧的质量分数约为21.6%,设该饱和一元醇的化学式为CnH2n+2O,氧元素的质量分数=$\frac{16}{14n+2+16}$,则n=4,且A中只有一个甲基,所以该一元醇是1-丁醇,在铜作催化剂、加热条件下,A被氧气氧化生成B丁醛,丁醛和氢氧化钠的水溶液发生反应生成 C,结合题给信息知,C的结构简式为:CH3CH2CH2CH=C(CH2CH3)CHO,C反应生成D,D的相对分子质量是130,则C和氢气发生加成反应生成D,则D的结构简式为:CH3CH2CH2CH2CH(CH2OH)CH2CH3,D和邻羟基苯甲酸发生酯化反应生成E,E的结构简式为: ,结合物质的结构和性质解答.
,结合物质的结构和性质解答.
解答 解:一元醇A中氧的质量分数约为21.6%,设该饱和一元醇的化学式为CnH2n+2O,氧元素的质量分数=$\frac{16}{14n+2+16}$,则n=4,且A中只有一个甲基,所以该一元醇是1-丁醇,在铜作催化剂、加热条件下,A被氧气氧化生成B丁醛,丁醛和氢氧化钠的水溶液发生反应生成 C,结合题给信息知,C的结构简式为:CH3CH2CH2CH=C(CH2CH3)CHO,C反应生成D,D的相对分子质量是130,则C和氢气发生加成反应生成D,则D的结构简式为:CH3CH2CH2CH2CH(CH2OH)CH2CH3,D和邻羟基苯甲酸发生酯化反应生成E,E的结构简式为: ,
,
(1)通过以上分析知,A的分子式为:C4H10O,结构分析显示A只有一个甲基,A的名称为1-丁醇,
故答案为:C4H10O,1-丁醇(或正丁醇);
(2)加热条件下,丁醛和新制氢氧化铜反应生成丁酸钠、氧化亚铜和水,反应方程式为:CH3CH2CH2CHO+2Cu(OH)2+NaOH $\stackrel{△}{→}$CH3CH2CH2COONa+Cu2O↓+3H2O,C中含有醛基和碳碳双键,都能和溴水反应,要检验两种官能团,则应先用银氨溶液检验醛基,然后再用溴水检验碳碳双键,所以所加试剂先后顺序是:银氨溶液、稀盐酸、溴水,
故答案为:CH3CH2CH2CHO+2Cu(OH)2+NaOH $\stackrel{△}{→}$CH3CH2CH2COONa+Cu2O↓+3H2O;银氨溶液、稀盐酸、溴水;
(3)C和氢气发生加成反应(或还原反应)生成D,C中的醛基被还原生成羟基,所以D中含有羟基,
故答案为:还原反应(或加成反应);羟基;
(5)a.分子中有6个碳原子在一条直线上,则该分子中含有两个碳碳三键:
b.分子中所含官能团包括水杨酸具有的官能团,则该分子中含有一个羟基和一个羧基,
所以水杨酸同分异构体的结构简式为:HOCH2C≡C-C≡CCH2COOH、 、HOCH2CH2C≡C-C≡C-COOH、
、HOCH2CH2C≡C-C≡C-COOH、 ,
,
故答案为:HOCH2C≡C-C≡CCH2COOH、 、HOCH2CH2C≡C-C≡C-COOH、
、HOCH2CH2C≡C-C≡C-COOH、 (其中两种);
(其中两种);
(6)第④步的反应是酯化反应,根据乙酸乙酯的反应条件知,该反应条件是浓硫酸作催化剂、加热,通过以上分析知,E的结构简式为: ,
,
故答案为:浓H2SO4、加热, .
.
点评 本题考查有机物的推断,正确推断出A物质是解本题关键,结合题给信息进行分析解答,难度中等,注意溴水能氧化醛基,为易错点.

| A. | 就地在田间焚烧秸秆,减少运输成本 | |
| B. | 烧煤进行脱硫、脱硝处理,减少空气污染 | |
| C. | 推广和鼓励多使用私家车出行 | |
| D. | 做好空气质量预报工作,以使污染程度高是好预防 |
| A. | 0.1mol/L醋酸钙溶液中,c (Ca 2+)>c(CH3COO-)>c(OH-)>c(H+) | |
| B. | 体积和pH 都相同的NH4Cl溶液、盐酸,完全溶解少量且等同的锌粉,前者用时少 | |
| C. | 将nmolH2(g)、nmol I2(g)和2nmolH2(g)、2nmolI2(g)分别充入两个恒温恒容的容器中,平衡时H2的转化率前者小于后者 | |
| D. | 某物质的溶液中由水电离出的c(H+)=1×10-amol/L,若a>7时,该溶液的pH一定为14-a |
| A. | CO(g)的燃烧热是283.0kJ/mol,则2CO2(g)═2CO(g)+O2(g)反应的△H=+2×283.0kJ/mol | |
| B. | HCl和NaOH反应的中和热△H=-57.3kJ/mol,则稀醋酸与稀NaOH溶液反应生成1 mol 水,放出57.3kJ热量 | |
| C. | 需要加热才能发生的反应一定是吸热反应 | |
| D. | 1mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热 |
(1)现有一瓶A和B的混合液,已知它们的性质如下表.
物质 | 熔点/℃ | 沸点/℃ | 密度/g•cm-3 | 溶解性 |
A | -11.5 | 198 | 1.11 | A、B互溶,且均易溶于水 |
B | 17.9 | 290 | 1.26 |
(2)在分液漏斗中用一种有机溶剂萃取水溶液里的某物质时,静置分层后,如果不知道哪一层液体是“水层”,试设计一种简便的判断方法.答:向分液漏斗中加入少量水,体积增大的液层是水层.
| A. | 常温下,将pH=2的HA溶液与pH=12的BOH溶液等体积混合后,溶液的pH<7,则BA为强酸弱碱盐 | |
| B. | 弱电解质溶液稀释后,溶液中各离子浓度一定都减小 | |
| C. | 常温下,向体积相同pH均为1的盐酸和醋酸溶液中分别加入足量锌片,两种溶液生成H2的体积相同 | |
| D. | 常温下,将pH均为13的NaOH溶液和氨水分别加水稀释100倍后,氨水的碱性强于NaOH溶液 |
| A. | 这是一个氧化还原反应,Na2O2既是氧化剂,又是还原剂 | |
| B. | 这是一个氧化还原反应,Na2O2是氧化剂,CO2是还原剂 | |
| C. | 这是一个氧化还原反应,Na2O2是还原剂,CO2是氧化剂 | |
| D. | 这是一个置换反应,有单质O2产生 |
 .
.