题目内容
下列与反应原理相关的叙述不正确的是( )
| A、装置Ⅰ的溶液若换为稀硝酸,则腐蚀过程与原装置不同 |
| B、装置Ⅱ在反应结束时溶液中存在Fe2+ |
| C、装置Ⅰ中不可能发生如下反应:Fe+2Fe3+═3Fe2+ |
| D、装置Ⅱ中的铁丝能发生电化学腐蚀 |
考点:金属的电化学腐蚀与防护
专题:电化学专题
分析:A、铁在浓硝酸中钝化,原电池中失电子的为负极;
B、II中发生吸氧腐蚀,U形管左端气体减少,液面升高;
C、当浓硝酸变为稀硝酸时,氧化铁溶解为铁离子;
D、铁丝中含碳,有电解质溶液及氧气,能构成原电池.
B、II中发生吸氧腐蚀,U形管左端气体减少,液面升高;
C、当浓硝酸变为稀硝酸时,氧化铁溶解为铁离子;
D、铁丝中含碳,有电解质溶液及氧气,能构成原电池.
解答:
解:A、铁在浓硝酸中钝化,Cu失电子作负极,换为稀硝酸时,Fe失电子作负极,故A正确;
B、II中发生吸氧腐蚀,U形管左端气体减少,液面升高,稀硫酸与Fe接触生成Fe2+,所以装置Ⅱ在反应结束时溶液中存在Fe2+,故B正确;
C、当浓硝酸变为稀硝酸时,氧化铁溶解为铁离子,发生Fe+2Fe3+═3Fe2+,故C错误;
D、铁丝中含碳,有电解质溶液及氧气,能构成原电池,所以装置Ⅱ中的铁丝能发生电化学腐蚀,故D在.
故选C.
B、II中发生吸氧腐蚀,U形管左端气体减少,液面升高,稀硫酸与Fe接触生成Fe2+,所以装置Ⅱ在反应结束时溶液中存在Fe2+,故B正确;
C、当浓硝酸变为稀硝酸时,氧化铁溶解为铁离子,发生Fe+2Fe3+═3Fe2+,故C错误;
D、铁丝中含碳,有电解质溶液及氧气,能构成原电池,所以装置Ⅱ中的铁丝能发生电化学腐蚀,故D在.
故选C.
点评:本题考查 原电池原理的应用,侧重于基础知识的考查,注意把握正负极的判断方法,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
短周期主族元素A、B、C、D、E的原子序数依次递增,A、B两元素相邻,B、C、E原子的最外层电子数之和为13,E原子最外层电子数是B原子内层电子数的3倍或者C原子最外层电子数的3倍,B、D原子最外层电子数之和等于C、E原子最外层电子数之和.下列说法正确的是( )
| A、元素B和E的氧化物对应的水化物均为强酸 |
| B、C的单质能与A的氧化物发生置换反应 |
| C、元素C、D、E的最高价氧化物对应的水化物之间均可相互反应 |
| D、工业上常用电解元素C、D的氯化物来制取它们的单质 |
下列化合物的俗称与化学式不对应的是( )
| A、绿矾:FeSO4?7H2O |
| B、小苏打:NaHCO3 |
| C、明矾:Al2(SO4)3?12H2O |
| D、胆矾:CuSO4?5H2O |
下列物质所发生的化学反应中,由于反应物的用量不同而得到不同产物的是( )
①铁与稀硝酸 ②AgNO3溶液与氨水溶液 ③碳酸钠溶液与稀盐酸 ④铁与氯气 ⑤NaAlO2溶液和稀盐酸 ⑥FeCl3溶液与Na2S溶液.
①铁与稀硝酸 ②AgNO3溶液与氨水溶液 ③碳酸钠溶液与稀盐酸 ④铁与氯气 ⑤NaAlO2溶液和稀盐酸 ⑥FeCl3溶液与Na2S溶液.
| A、全部都是 | B、①②③⑤⑥ |
| C、①②③⑤ | D、③④⑤ |
下列各电子式中正确的是( )
A、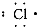 氯原子 |
B、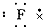 氟原子 |
C、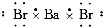 溴化钡 |
D、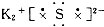 硫化钾 |
下列各组微粒在溶液中不能大量共存的是( )
①Fe3+、K+、Cl-、OH- ②Na+、H+、SO42-、HCO3-
③Mg2+、Fe3+、H+、Cl- ④Ag+、Na+、Cu2+、Cl-.
①Fe3+、K+、Cl-、OH- ②Na+、H+、SO42-、HCO3-
③Mg2+、Fe3+、H+、Cl- ④Ag+、Na+、Cu2+、Cl-.
| A、②③④ | B、①③ |
| C、①②④ | D、①②③ |
液体颜色不呈砖红色的原因是( )
| A、淀粉酶在40℃时活性相对较高 |
| B、淀粉酶催化淀粉水解产生的无还原糖 |
| C、淀粉酶与新制氢氧化铜反应 |
| D、淀粉酶在100℃时失活 |
已知在101kPa时:CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-820kJ?mol-1.则下列说法正确的是( )
| A、CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H>-820 kJ?mol-1 |
| B、CH4的燃烧热是820kJ?mol-1 |
| C、1mol CH4和2mol O2的键能之和大于1mol CO2和2mol H2O的键能之和 |
| D、11.2L(标准状况)CH4完全燃烧生成气态水时放出410kJ热量 |
我们所吃的豆腐,主要成分是( )
| A、葡萄糖 | B、蛋白质 |
| C、脂肪 | D、淀粉 |