题目内容
下列物质既有氧化性又有还原性的是( )
| A、HCl |
| B、Fe |
| C、Cl- |
| D、Na+ |
考点:氧化还原反应
专题:氧化还原反应专题
分析:处于最高价态的元素只有氧化性,处于最低价态的元素只有还原性,处于中间价态的元素既有氧化性又有还原性.
解答:
解:A.HCl中H元素处于最高价态,所以H元素只有氧化性,Cl元素处于最低价态,所以Cl只有还原性,则HCl既有氧化性也有还原性,故A正确;
B.Fe元素处于最低价态,所以只有还原性,故B错误;
C.Cl-中Cl元素处于最低价态,所以只有还原性,故C错误;
D.Na+中Na元素处于最高价态,所以只有氧化性,故D错误;
故选A.
B.Fe元素处于最低价态,所以只有还原性,故B错误;
C.Cl-中Cl元素处于最低价态,所以只有还原性,故C错误;
D.Na+中Na元素处于最高价态,所以只有氧化性,故D错误;
故选A.
点评:本题考查了氧化还原反应,明确元素化合价与元素氧化性还原性的关系是解本题关键,根据元素化合价高低判断即可,题目难度不大.

练习册系列答案
相关题目
某同学写出的下列烷烃的名称中,不符合系统命名法的是( )
| A、2,3-二甲基丁烷 |
| B、2,2,3,3-四甲基丁烷 |
| C、2-甲基丙烷 |
| D、2-甲基-2-乙基丁烷 |
下列说法正确的是( )
| A、氧化还原反应的本质是元素化合价发生变化 |
| B、还原剂是一种能够得到电子的物质 |
| C、物质所含元素化合价降低的反应是氧化反应 |
| D、氧化反应和还原反应是同时发生的 |
下列选项中所涉及的两个量一定相等的是( )
| A、11.2 L N2与14 g CO气体所含有的原子数 |
| B、电解精炼铜时阳极溶解与阴极析出的铜的质量 |
| C、6.2 g Na2O和7.8 g Na2O2中所含的离子数 |
| D、1.8g重水(D2O,D为12H)中含有的中子数为6.02×1022 |
下列溶液中,物质的量浓度最大的是( )
| A、将40gNaOH溶于水并配成1L的溶液 |
| B、0.5 L含49gH2SO4的溶液 |
| C、将1molNa2O 溶于水并配成1L的溶液 |
| D、含K+为1mol?L-1的K2SO4溶液 |
完全沉淀等物质的量浓度的NaCl、MgCl2、AlCl3溶液中的Cl-,消耗等物质的量浓度的AgNO3溶液的体积比为2:3:6,则上述溶液的体积比为( )
| A、1:1:1 |
| B、3:2:1 |
| C、6:3:2 |
| D、4:3:4 |
在密闭容器中充入4molSO2和3molO2,一定条件下平衡:2SO2(g)+O2(g)?2SO3(g)△H=-a kJ/mol,反应中测得SO2的转化率为90%,则在此条件下反应放出的热量( )
| A、1.8a kJ |
| B、a kJ |
| C、2a kJ |
| D、0.9a kJ |
在体积一定的密闭容器中加入一定量的物质A、B、C,在一定条件下发生反应建立的化学平衡:aA(g)+bB(g)?xC(g),符合如图所示的关系(c%表示平衡混合气中产物C的百分含量,T表示温度,p表示压强).在图中,Y轴是指( )
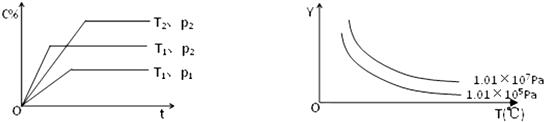

| A、反应物A的百分含量 |
| B、反应体系内分子的总数目 |
| C、平衡混合气体的密度 |
| D、平衡混合气体的平均摩尔质量 |