题目内容
10. 有A、B、C、D、E五种短周期元素,且相邻的A、B、C、D四种元素原子核外共有56个电子,在周期表中的位置如图所示.E的氢氧化物是两性氢氧化物;E的阳离子与A的阴离子核外电子层结构相同.请回答下列问题:
有A、B、C、D、E五种短周期元素,且相邻的A、B、C、D四种元素原子核外共有56个电子,在周期表中的位置如图所示.E的氢氧化物是两性氢氧化物;E的阳离子与A的阴离子核外电子层结构相同.请回答下列问题:(1)A在元素周期表中的位置第二周期第ⅥA族.
B的最高价氧化物化学式为P2O5.
写出C元素气态氢化物的电子式
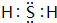 .
.(2)D的单质与水反应的化学方程式为Cl2+H2O=HCl+HClO.
(3)五种元素中原子半径最小的是O(填元素符号),这些元素的最高价氧化物的对应水化物中HClO4酸性最强.
(4)C的一种氧化物是常见的大气污染物.为防止大气污染,某化工厂用NaOH溶液、石灰和O2处理含C的上述氧化物的尾气,使其转化为石膏(CaSO4•2H2O).假设在转化过程中C元素不损失,每天处理1120m3(标准状况下)含2%(体积分数)上述氧化物的尾气,理论上可以得到多少千克石膏(请写出计算过程).
分析 A、B、C、D、E五种短周期元素,根据元素在周期表中的位置知,A为第二周期元素,B、C、D为第三周期元素,设C的原子序数为x,则A的原子序数为x-8,B的原子序数为x-1,D的原子序数为x+1,相邻的A、B、C、D四种元素原子核外共有56个电子,则x-8+x-1+x+x+1=56,则x=16,所以C为S元素、A为O元素、B为P元素、D为Cl元素,E的氢氧化物是两性氢氧化物,E的阳离子与A的阴离子核外电子层结构相同,则E为Al元素,再结合物质结构、物质性质分析解答.
解答 解:A、B、C、D、E五种短周期元素,根据元素在周期表中的位置知,A为第二周期元素,B、C、D为第三周期元素,设C的原子序数为x,则A的原子序数为x-8,B的原子序数为x-1,D的原子序数为x+1,相邻的A、B、C、D四种元素原子核外共有56个电子,则x-8+x-1+x+x+1=56,则x=16,所以C为S元素、A为O元素、B为P元素、D为Cl元素,E的氢氧化物是两性氢氧化物,E的阳离子与A的阴离子核外电子层结构相同,则E为Al元素,
(1)A为O元素,在周期表中位置:第二周期第ⅥA族,
B为P元素,最高价氧化物化学式为P2O5,
C元素气态氢化物为H2S,电子式为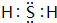 ,
,
故答案为:第二周期第ⅥA族;P2O5;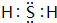 ;
;
(2)氯气与水反应方程式为:Cl2+H2O=HCl+HClO,
故答案为:Cl2+H2O=HCl+HClO;
(3)同一周期随原子半径随着原子序数增大原子半径减小,一般原子电子层数越多原子半径越大,故原子半径从小到大的顺序为O<Cl<S<P<Al,这些元素的最高价氧化物的对应水化物中HClO4酸性最强,
故答案为:O;HClO4;
(4)尾气中C的氧化物SO2的物质的量为$\frac{1120×1{0}^{3}L}{22.4L/mol}$×2%=1000mol,根据S元素守恒n(CaSO4•2H2O)=1000mol,故m(CaSO4•2H2O)=1000mol×172g/mol=173000g=172Kg,
故:理论上可以得到172千克石膏.
点评 本题考查了元素周期表和元素周期律的综合应用,涉及元素推断、物质的性质、元素周期律、化学计算等,正确推断元素是解本题关键,(4)中注意利用原子守恒解答.

| A. | 新制碱性Cu(OH)2悬浊液 | B. | FeCl3溶液 | ||
| C. | BaCl2溶液 | D. | 酸性KMnO4溶液 |
| A. | 用苯萃取碘水中的碘时,将碘的苯溶液从分液漏斗下口放出 | |
| B. | Na2SiO3溶液中通入CO2,溶液变浑浊,继续通CO2至过量,浑浊消失 | |
| C. | 用铂丝蘸取少量某溶液进行焰色反应,火焰呈黄色,该溶液一定是钠盐溶液 | |
| D. | NaCl溶液蒸发结晶时,蒸发皿中有晶体析出并剩余少量液体即停止加热 |
| A. | 各物质的浓度之比c(A):c(B):c(C)=2:3:4 | |
| B. | 平衡混合气体中各物质的浓度相等 | |
| C. | 平衡混合气的体积是反应开始前的$\frac{4}{5}$ | |
| D. | 单位时间内,若消耗了a mol A物质,同时也消耗了2a mol C物质 |
已知:生成氢氧化物沉淀的pH
| Mn(OH)2 | Fe(OH)2 | Fe(OH)3 | Cu(OH)2 | |
| 开始沉淀时 | 8.3 | 6.3 | 2.7 | 4.7 |
| 完全沉淀时 | 9.8 | 8.3 | 3.7 | 6.7 |
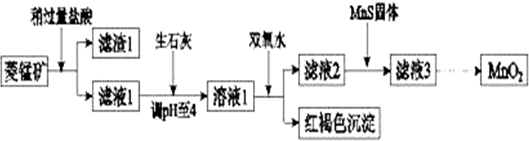
(1)含杂质的菱锰矿使用前需将其粉碎,主要目的是增大接触面积,提高反应速率.盐酸溶解MnCO3的化学方程式是MnCO3+2HCl=MnCl2+CO2↑+H2O.
(2)向溶液1中加入双氧水时,反应的离子方程式是2Fe2++H2O2+4H2O=2Fe(OH)3↓+4H+.
(3)滤液2中加入稍过量的难溶电解质MnS,以除去Cu2+,反应的离子方程式是MnS+Cu2+=Mn2++CuS.
(4)将MnCl2转化为MnO2的一种方法是氧化法.其具体做法是用酸化的NaClO3溶液将MnCl2氧化,该反应的离子方程式为:□Mn2++□ClO3-+□4H2O=□Cl2+□5MnO2+□8H+.
(5)将MnCl2转化为MnO2的另一种方法是电解法.
①阳极生成MnO2的电极反应式是Mn2+-2e-+2H2O=MnO2+4H+.
②若直接电解MnCl2溶液,生成MnO2的同时会产生少量Cl2.检验Cl2的操作是将润湿的淀粉碘化钾试纸置于阳极附近,若试纸变蓝则证明有Cl2生成.
③若在上述MnCl2溶液中加入一定量的Mn(NO3)2粉末,则无Cl2产生.其原因是其它条件不变下,增大Mn2+浓度或增大$\frac{c(M{n}^{2+})}{c(C{l}^{-})}$,有利于Mn2+放电(不利于Cl-放电)..
 科学家已获得了极具理论研究意义的N4分子,其结构为正四面体(如图所示),与白磷分子相似.气态时,已知断裂1mol N-N键吸收167kJ热量,断裂1mol N≡N键吸收942kJ热量,则( )
科学家已获得了极具理论研究意义的N4分子,其结构为正四面体(如图所示),与白磷分子相似.气态时,已知断裂1mol N-N键吸收167kJ热量,断裂1mol N≡N键吸收942kJ热量,则( )| A. | N4与N2互称为同位素 | |
| B. | N4属于一种新型的化合物 | |
| C. | N4化学性质比N2稳定 | |
| D. | 1mol N4气体转化为N2时要放出882kJ能量 |

 HCOOCH3+H2O
HCOOCH3+H2O