题目内容
2.在标准状况下,O2与H2的密度之比为( )| A. | 4:1 | B. | 8:1 | C. | 32:1 | D. | 16:1 |
分析 由ρ=$\frac{M}{Vm}$可知,标准状况下Vm相同,密度之比等于摩尔质量之比,以此来解答.
解答 解:标准状况下Vm相同,密度之比等于摩尔质量之比,则O2与H2的密度之比为32g/mol:2g/mol=16:1,
故选D.
点评 本题考查物质的量的计算,为高频考点,把握密度与摩尔质量的关系为解答的关键,侧重分析与计算能力的考查,注意Vm相同,题目难度不大.

练习册系列答案
 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案
相关题目
13.在酸性高锰酸钾溶液中加入Na2O2粉末,高锰酸钾溶液褪色,其中发生反应的离子方程式为:2MnO4-+16H++5Na2O2═2Mn2++5O2↑+8H2O+10Na+下列判断正确的是( )
| A. | 高锰酸钾是氧化剂,Na2O2既是氧化剂,又是还原剂 | |
| B. | 反应的氧化产物Mn2+ | |
| C. | 当反应产生标准状况下2.24L O2 时,反应转移的电子为0.2mol | |
| D. | 向高锰酸钾溶液滴加浓盐酸可以得到酸性高锰酸钾溶液 |
10.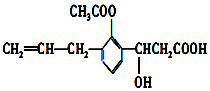 有机物的结构简式如图,则此有机物可发生的反应类型有( )
有机物的结构简式如图,则此有机物可发生的反应类型有( )
①取代
②加成
③消去
④酯化
⑤水解
⑥氧化
⑦中和
⑧加聚.
 有机物的结构简式如图,则此有机物可发生的反应类型有( )
有机物的结构简式如图,则此有机物可发生的反应类型有( ) ①取代
②加成
③消去
④酯化
⑤水解
⑥氧化
⑦中和
⑧加聚.
| A. | ①②③⑤⑥ | B. | ②③④⑤⑥⑧ | C. | ②③④⑤⑥⑦ | D. | ①②③④⑤⑥⑦⑧ |