题目内容
13.在酸性高锰酸钾溶液中加入Na2O2粉末,高锰酸钾溶液褪色,其中发生反应的离子方程式为:2MnO4-+16H++5Na2O2═2Mn2++5O2↑+8H2O+10Na+下列判断正确的是( )| A. | 高锰酸钾是氧化剂,Na2O2既是氧化剂,又是还原剂 | |
| B. | 反应的氧化产物Mn2+ | |
| C. | 当反应产生标准状况下2.24L O2 时,反应转移的电子为0.2mol | |
| D. | 向高锰酸钾溶液滴加浓盐酸可以得到酸性高锰酸钾溶液 |
分析 该反应中Mn元素化合价由+7价变为+2价、O元素化合价由-1价变为0价,所以MnO4-是氧化剂、Na2O2是还原剂,根据氧气和转移电子之间的关系式计算.
解答 解:A.该反应中Mn元素化合价由+7价变为+2价、O元素化合价由-1价变为0价,所以MnO4-是氧化剂、Na2O2是还原剂,故A错误;
B.过氧化钠是还原剂,则氧化产物是氧气,故B错误;
C.生成标况下2.24L氧气时,转移电子的物质的量=$\frac{2.24L}{22.4L/mol}$×2=0.2mol,故C正确;
D.高锰酸钾能氧化浓盐酸生成氯气,所以不能将浓盐酸滴入高锰酸钾溶液中,应该用稀硫酸,故D错误;
故选C.
点评 本题考查氧化还原反应,题目难度不大,侧重考查学生对基本概念、基本理论的分析解答,注意高锰酸钾的强氧化性,易错选项是D.

练习册系列答案
相关题目
5.将一定质量的硝酸铵,置于真空中,加热至300℃使其完全分解,分解方程式为:2NH4NO3=2N2+O2+4H2O,混合气体的平均摩尔质量为( )
| A. | 22.9g/mol | B. | 26 | C. | 26 g/mol | D. | 29.3 g/mol |
4.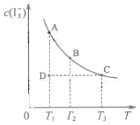 I2在KI溶液中存在下列平衡:I2(aq)+I-(aq)?I3-(aq)某I2、KI混合溶液中,I3-的物质的量浓度c(I3-)与温度T的关系如图所示(曲线上任何一点都表示平衡状态,忽略I2 的挥发).下列说法正确的是( )
I2在KI溶液中存在下列平衡:I2(aq)+I-(aq)?I3-(aq)某I2、KI混合溶液中,I3-的物质的量浓度c(I3-)与温度T的关系如图所示(曲线上任何一点都表示平衡状态,忽略I2 的挥发).下列说法正确的是( )
 I2在KI溶液中存在下列平衡:I2(aq)+I-(aq)?I3-(aq)某I2、KI混合溶液中,I3-的物质的量浓度c(I3-)与温度T的关系如图所示(曲线上任何一点都表示平衡状态,忽略I2 的挥发).下列说法正确的是( )
I2在KI溶液中存在下列平衡:I2(aq)+I-(aq)?I3-(aq)某I2、KI混合溶液中,I3-的物质的量浓度c(I3-)与温度T的关系如图所示(曲线上任何一点都表示平衡状态,忽略I2 的挥发).下列说法正确的是( )| A. | 反应 I2(aq)+I-(aq)?I3-(aq)△H>0 | |
| B. | 状态A与状态B相比,状态A的c(I2)大 | |
| C. | 若反应进行到状态D时,一定有v逆>v正 | |
| D. | 若温度为T1、T2,反应的平衡常数K1、K2则 K1>K2 |
5.某温度下,在一容积可变的容器中,反应2A(g)+B(g)?2C(g)达到平衡时,A、B和C的物质的质量的量分别为4mol、2mol和4mol,保持温度和压强不变,对平衡混合物中三者的物质的量做如下调整,可使平衡右移的是( )
| A. | 均减半 | B. | 均加倍 | C. | 均减少1mol | D. | 均增加1mol |
2.在标准状况下,O2与H2的密度之比为( )
| A. | 4:1 | B. | 8:1 | C. | 32:1 | D. | 16:1 |
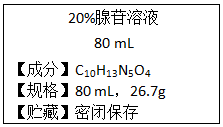 根据腺苷的相关信息,计算下列各题:
根据腺苷的相关信息,计算下列各题: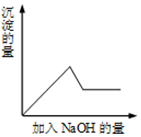 有一无色溶液,其中可能含有Fe3+、Cu2+、K+、Al3+、Mg2+、SO42-、Cl-等离子中的几种,为分析其成分,取此溶液分别进行了三个实验,其操作和有关现象如下:
有一无色溶液,其中可能含有Fe3+、Cu2+、K+、Al3+、Mg2+、SO42-、Cl-等离子中的几种,为分析其成分,取此溶液分别进行了三个实验,其操作和有关现象如下: