��Ŀ����
 ��1��������Ϊһ��������Դ����ȼ����ֵ�ߡ���Դ�ḻ��ȼ�ղ�������Ⱦ���ŵ㣮��֪ȼ��4g H2����Һ̬ˮʱ����Ϊ571.6kJ����д����ʾH2ȼ���ȵ��Ȼ�ѧ����ʽ
��1��������Ϊһ��������Դ����ȼ����ֵ�ߡ���Դ�ḻ��ȼ�ղ�������Ⱦ���ŵ㣮��֪ȼ��4g H2����Һ̬ˮʱ����Ϊ571.6kJ����д����ʾH2ȼ���ȵ��Ȼ�ѧ����ʽ��2��Ŀǰ��ҵ��ͨ��������ˮú���ķ�����ã���Ӧ�Ļ�ѧ����Ϊ��
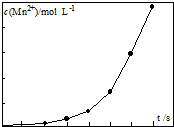
CO��g��+H2O��g���TCO2��g��+H2��g����H��0������ijһ�ݻ�Ϊ4L���ܱ������ڣ�����2.0mol��CO��3.0mol��H2O��g�����ڴ������ڵ���������850����¼��ȣ�����������Ӧ����Ӧ��CO2��Ũ����ʱ��仯�������ͼ��ʾ���ٸ�����ͼ���ݣ���������850��ʱ�÷�Ӧ�Ļ�ѧƽ�ⳣ��K��850�棩=
��ƽ��ʱCO��ת������
��3�����÷�Ӧ����750��ʱ�ﵽ��ѧƽ��״̬�����ʱ��ƽ�ⳣ��K��750�棩
��4��850��ʱ������һ�ݻ��ɱ���ܱ�������ͬʱ����1.0mol CO��3.0mol H2O��g����1.0mol��CO2��x mol H2����
�ٵ�x=5.0ʱ��������Ӧ��
����Ҫʹ������Ӧ��ʼ������Ӧ������У���xӦ�����������
����850��ʱ������x=5.0��x=6.0���������ʵ�Ͷ�ϲ��䣬��������Ӧ�ﵽƽ����H2����������ֱ�Ϊa%��b%����a
���㣺�Ȼ�ѧ����ʽ,���ʵ�����Ũ����ʱ��ı仯����,��ѧƽ��ļ���
ר�⣺��ѧ��Ӧ�е������仯,��ѧƽ��ר��
��������1��4g H2�����ʵ�����2mol��4g H2ȼ������Һ̬ˮʱ����Ϊ571.6kJ����1molȼ������Һ̬ˮʱ����Ϊ285.8kJ��
��2������ƽ�ⳣ��ָ��������Ũ�ȵĻ�ѧ���������ݵij˻����Ը���Ӧ��Ũ�ȵĻ�ѧ���������ݵij˻����õı�ֵ���н��ƽ��ʱCO��ת���ʵ���ת��������ʼ��֮�ȣ�
��3������Ӧ���ȣ�������ƽ�����ƣ�ƽ�ⳣ����С��
��4���ٷ�Ӧ���������ʵ���ϵ����ͬ��Ϊ1���������ʵ�������Ũ�ȣ�����Ũ����Qc������Ũ����Qc��ƽ�ⳣ��k�Ĺ�ϵ�жϣ�Qc��kƽ�����淴Ӧ���У�Qc=k��Ӧ����ƽ��״̬��Qc��kƽ��������Ӧ���У�
����x��ʾ��Ũ����Qc��ƽ��������Ӧ�ƶ���Ӧ����Ũ����Qc��k���ݴ˼����жϣ�
������һ������������������������ƽ�����淴Ӧ�����ƶ���ƽ���ƶ��Ľ���ǽ�����������ķ��ȣ���ƽ�������������������Ǵ���ԭ���ģ�
��2������ƽ�ⳣ��ָ��������Ũ�ȵĻ�ѧ���������ݵij˻����Ը���Ӧ��Ũ�ȵĻ�ѧ���������ݵij˻����õı�ֵ���н��ƽ��ʱCO��ת���ʵ���ת��������ʼ��֮�ȣ�
��3������Ӧ���ȣ�������ƽ�����ƣ�ƽ�ⳣ����С��
��4���ٷ�Ӧ���������ʵ���ϵ����ͬ��Ϊ1���������ʵ�������Ũ�ȣ�����Ũ����Qc������Ũ����Qc��ƽ�ⳣ��k�Ĺ�ϵ�жϣ�Qc��kƽ�����淴Ӧ���У�Qc=k��Ӧ����ƽ��״̬��Qc��kƽ��������Ӧ���У�
����x��ʾ��Ũ����Qc��ƽ��������Ӧ�ƶ���Ӧ����Ũ����Qc��k���ݴ˼����жϣ�
������һ������������������������ƽ�����淴Ӧ�����ƶ���ƽ���ƶ��Ľ���ǽ�����������ķ��ȣ���ƽ�������������������Ǵ���ԭ���ģ�
���
�⣺��1��4g H2�����ʵ�����2mol��4g H2ȼ������Һ̬ˮʱ����Ϊ571.6kJ����1molȼ������Һ̬ˮʱ����Ϊ285.8kJ����������ȼ���Ȼ�ѧ����ʽΪH2��g��+
O2��g���TH2O��l����H=-285.6 kJ?mol-1���ʴ�Ϊ��H2��g��+
O2��g���TH2O��l����H=-285.6 kJ?mol-1��
��2������������ʽ�����㣬
CO��g��+H2O��g��?CO2��g��+H2��g��
��ʼŨ��/mol?L-1 ��
0 0
ת��Ũ��/mol?L-1 ��0.3 0.3 0.3 0.3
ƽ��Ũ��/mol?L-1 ��0.2 0.45 0.3 0.3
��ƽ�ⳣ�������������Ũ����֮�����Է�Ӧ���Ũ����֮��������K��850�棩=
=
=1��
�ʴ�Ϊ��1��
��ƽ��ʱCO��ת����=
��100%=60%���ʴ�Ϊ��60%��
��3��CO��g��+H2O��g���TCO2��g��+H2��g����H��0������Ӧ���ȣ�������ƽ�����ƣ�ƽ�ⳣ����С��K��750�棩����K��850�棩���ʴ�Ϊ�����ڣ�
��4���ٴ�ʱ��Ũ����Qc=
=1.67������ƽ�ⳣ��1����ƽ�����淴Ӧ�����ƶ����ʴ�Ϊ���淴Ӧ��
��ƽ��������Ӧ�����ƶ���Ũ����С��ƽ�ⳣ������
��1�����x��3���ʴ�Ϊ��x��3��
�ۼ���6mol�����������ƽ�⣬���Ե�ЧΪ�ڼ���5mol��������ƽ����ټ���1mol����������һ������������������������ƽ�����淴Ӧ�����ƶ���ƽ���ƶ��Ľ���ǽ�����������ķ��ȣ���ƽ�������������������Ǵ���ԭ���ģ��ʵ�H2����������ֱ�Ϊa%��b%���ʴ�Ϊ��С�ڣ�
| 1 |
| 2 |
| 1 |
| 2 |
��2������������ʽ�����㣬
CO��g��+H2O��g��?CO2��g��+H2��g��
��ʼŨ��/mol?L-1 ��
| 2 |
| 4 |
| 3 |
| 4 |
ת��Ũ��/mol?L-1 ��0.3 0.3 0.3 0.3
ƽ��Ũ��/mol?L-1 ��0.2 0.45 0.3 0.3
��ƽ�ⳣ�������������Ũ����֮�����Է�Ӧ���Ũ����֮��������K��850�棩=
| c(CO2)c(H2) |
| c(CO)c(H2O) |
| 0.3��0.3 |
| 0.2��0.45 |
�ʴ�Ϊ��1��
��ƽ��ʱCO��ת����=
| 0.3 |
| 0.5 |
��3��CO��g��+H2O��g���TCO2��g��+H2��g����H��0������Ӧ���ȣ�������ƽ�����ƣ�ƽ�ⳣ����С��K��750�棩����K��850�棩���ʴ�Ϊ�����ڣ�
��4���ٴ�ʱ��Ũ����Qc=
| 1��5 |
| 1��3 |
��ƽ��������Ӧ�����ƶ���Ũ����С��ƽ�ⳣ������
| 1��x |
| 1��3 |
�ۼ���6mol�����������ƽ�⣬���Ե�ЧΪ�ڼ���5mol��������ƽ����ټ���1mol����������һ������������������������ƽ�����淴Ӧ�����ƶ���ƽ���ƶ��Ľ���ǽ�����������ķ��ȣ���ƽ�������������������Ǵ���ԭ���ģ��ʵ�H2����������ֱ�Ϊa%��b%���ʴ�Ϊ��С�ڣ�
���������⿼��ת���ʡ���ѧƽ���йؼ��㡢��ѧƽ���ƶ���Ӱ�����صȣ�ע��ƽ�ⳣ����Ӧ�á�ƽ���ƶ��ı����ǽ��Ĺؼ�����Ŀ�Ѷ��еȣ�

��ϰ��ϵ�д�
 ��ʦָ����ĩ��̾�ϵ�д�
��ʦָ����ĩ��̾�ϵ�д�
�����Ŀ
�������ʺ����������ǣ�������
| A��1.204��1024��O2 |
| B��3molCO2 |
| C����״����89.6LCl2 |
| D��90gˮ |
�������йس����еij����������������в�����������ԭ��Ӧ���ǣ�������
| A���ղ��ù��������������ó����ֺ���ɫ��� |
| B���ô����ȥˮ������е�ˮ��[��Ҫ�ɷ�CaCO3] |
| C����ú����ȼ������[��Ҫ�ɷּ��飨CH4��]Ϊ�����ṩ���� |
| D��ţ�̾��ñ��ʸ��� |
 �����̿��Ʊ�������ص���Ҫ��Ӧ���£�
�����̿��Ʊ�������ص���Ҫ��Ӧ���£� ��Ԫ�����ڱ��У�ijϡ������Ԫ��ԭ�ӵ��������ӹ���Ϊ4s24p6������ͬ���ڵ� A��B��C��D����Ԫ�أ����ǵ�ԭ����������������Ϊ2��2��1��7������A��C��Ԫ��ԭ�ӵĴ���������Ϊ8��B��D��Ԫ ��ԭ�ӵĴ���������Ϊ18��E��D��Ԫ�ش���ͬ�壬���ڸ���Ԫ���У�E����̬�⻯��ķе���ߣ�
��Ԫ�����ڱ��У�ijϡ������Ԫ��ԭ�ӵ��������ӹ���Ϊ4s24p6������ͬ���ڵ� A��B��C��D����Ԫ�أ����ǵ�ԭ����������������Ϊ2��2��1��7������A��C��Ԫ��ԭ�ӵĴ���������Ϊ8��B��D��Ԫ ��ԭ�ӵĴ���������Ϊ18��E��D��Ԫ�ش���ͬ�壬���ڸ���Ԫ���У�E����̬�⻯��ķе���ߣ�