题目内容
下列反应属于吸热反应的是( )
| A、过氧化氢在MnO2催化条件下分解 |
| B、碳不完全燃烧产生CO |
| C、氢氧化钡晶体与氯化铵混合 |
| D、盐酸与氢氧化钠溶液反应 |
考点:吸热反应和放热反应
专题:化学反应中的能量变化
分析:常见的放热反应有:所有的物质燃烧、所有金属与酸反应、金属与水反应、所有中和反应、绝大多数化合反应和铝热反应;
常见的吸热反应有:绝大数分解反应(双氧水分解是放热反应)、个别的化合反应(如C和CO2)、置换以及某些复分解反应(如铵盐和强碱).
常见的吸热反应有:绝大数分解反应(双氧水分解是放热反应)、个别的化合反应(如C和CO2)、置换以及某些复分解反应(如铵盐和强碱).
解答:
解:A.过氧化氢在MnO2催化条件下分解是放热反应,故A错误;
B.碳不完全燃烧产生CO,燃烧是氧化反应,属于放热反应,故B错误,
C.氢氧化钡晶体与氯化铵混合属于吸热反应,故C正确;
D.盐酸与氢氧化钠溶液发生中和反应,属于放热反应,故D错误;
故选:C.
B.碳不完全燃烧产生CO,燃烧是氧化反应,属于放热反应,故B错误,
C.氢氧化钡晶体与氯化铵混合属于吸热反应,故C正确;
D.盐酸与氢氧化钠溶液发生中和反应,属于放热反应,故D错误;
故选:C.
点评:本题考查吸热反应,难度不大.抓住中学化学中常见的吸热或放热的反应是解题的关键.

练习册系列答案
 初中学业考试导与练系列答案
初中学业考试导与练系列答案
相关题目
氢化铵(NH4H)与氯化铵的结构相似,又知NH4H与水反应有氢气放出,下列叙述不正确的是( )
| A、NH4H是离子化合物,含有离子键和共价键 |
| B、NH4H溶于水,所形成的溶液成酸性 |
| C、NH4H与水反应时,NH4H是还原剂 |
| D、NH4H投入少量的水中,有两种气体产生 |
甲、乙两物质的溶解度曲线如图所示,下列叙述中正确的是( )
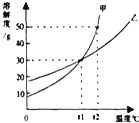

| A、t1℃时,甲、乙各30g分别加入70g水中均能恰好完全溶解 |
| B、t1℃时,甲和乙的饱和溶液中溶质的质量分数相等 |
| C、t2℃时,分别在100g水中各溶解20g甲、乙,同时降低温度,甲先达到饱和 |
| D、t2℃时,在100g水中放入60g甲,所得溶液溶质的质量分数为37.5% |
2003年2月1日,美国“哥伦比亚”号航天飞机在空中失事.有专家分析认为,其原因可能是航天飞机机壳底部的石墨瓦在空中脱落,击中机翼.航天飞机表面覆盖石墨瓦可以起隔热和保护作用,这主要是因为石墨( )
| A、能导电 |
| B、熔点高、耐高温,化学性质稳定 |
| C、密度小 |
| D、硬度小,有润滑作用 |
下列各种环境下的离子组合能够大量共存的是( )
| A、使pH试纸变红的溶液中:Fe2+、I-、NO3-、ClO- |
| B、中性溶液中:Mg2+、Fe3+、SO32-、Cl- |
| C、pH=0的溶液中:Al3+、NH4+、Ca2+、ClO- |
| D、c(H+)=10-14mol?L-1的溶液中,Na+、AlO2-、S2-、SO32- |
已知稀溶液中,强酸与强碱反应的中和热的热化学方程式为:H+(aq)+OH-(aq)=H2O(l),△H=-57.3kJ?mol-1.下列各反应放出的热量为57.3kJ的是( )
A、
| ||||||
| B、CH3COOH(aq)+KOH(aq)=CH3COOK(aq)+H2O(l) | ||||||
| C、HNO3(浓)+NaOH(aq)=NaNO3(aq)+H2O(l) | ||||||
D、HCl(aq)+
|
下列关于蛋白质性质的叙述中正确的是( )
| A、在蛋白质溶液中加入饱和硫酸铵溶液,蛋白质析出,虽再加水,也不溶解 |
| B、所有的蛋白质都能溶于水 |
| C、浓硝酸溅在皮肤上能使皮肤呈现黄色,是由于浓硝酸和蛋白质发生了颜色反应 |
| D、向鸡蛋清中加入食盐,会使蛋白质凝固变性 |
下列各组物质的性质排列不正确的是( )
| A、酸性:H2CO3>H3BO3>Al(OH)3 |
| B、溶液中结合质子的能力:O2->S2->Cl- |
| C、分散质粒子直径:胶体>浊液>溶液 |
| D、热稳定性:HF>H2O>NH3 |