题目内容
氢化铵(NH4H)与氯化铵的结构相似,又知NH4H与水反应有氢气放出,下列叙述不正确的是( )
| A、NH4H是离子化合物,含有离子键和共价键 |
| B、NH4H溶于水,所形成的溶液成酸性 |
| C、NH4H与水反应时,NH4H是还原剂 |
| D、NH4H投入少量的水中,有两种气体产生 |
考点:铵盐,氧化还原反应
专题:元素及其化合物
分析:A.NH4H是铵根离子与氢负离子通过离子键形成的离子化合物,属于离子晶体;
B.NH4H与水发生了氧化还原反应,NH4H+H20=NH3?H20+H2↑,生成的NH3?H20;
C.NH4H与水发生了氧化还原反应,氢负离子化合价升高;
D.NH4H固体投入少量的水中,由于发生的氧化还原反应是放热的,生成的NH3?H20分解为NH3和H20,所以可以得到两种气体.
B.NH4H与水发生了氧化还原反应,NH4H+H20=NH3?H20+H2↑,生成的NH3?H20;
C.NH4H与水发生了氧化还原反应,氢负离子化合价升高;
D.NH4H固体投入少量的水中,由于发生的氧化还原反应是放热的,生成的NH3?H20分解为NH3和H20,所以可以得到两种气体.
解答:
解:A.NH4H与氯化铵的结构相似,是由NH4+和H-构成的离子化合物,故A正确;
B.NH4H与水反应有H2和氨气生成,溶液呈碱性,故B错误;
C.NH4H与水发生了氧化还原反应,氢负离子化合价升高,被氧化,做还原剂,故C正确;
D.NH4H与水反应有H2生成,同时还会生成氨气,故D正确;
故选:C.
B.NH4H与水反应有H2和氨气生成,溶液呈碱性,故B错误;
C.NH4H与水发生了氧化还原反应,氢负离子化合价升高,被氧化,做还原剂,故C正确;
D.NH4H与水反应有H2生成,同时还会生成氨气,故D正确;
故选:C.
点评:本题考查了铵盐的结构和性质,侧重氧化还原反应迁移应用能力的考查,明确反应中元素的化合价变化为解答的关键,题目难度不大》

练习册系列答案
相关题目
化学中常用图象直观地描述化学反应的进程或结果.下列对图象的叙述正确的是( )
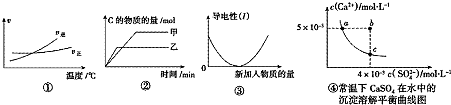

| A、根据图①可判断可逆反应A2(g)+3B2(g)?2AB2(g),正反应是吸热反应 |
| B、图②可表示压强对反应2A(g)+2B(g)?3C(g)+D(s)的影响,乙的压强大 |
| C、图③可表示乙酸溶液中通人氨气至过量的过程中溶液导电性的变化 |
| D、根据图④可知,a点对应的KSP等于c点对应的KSP |
用铂丝蘸取氯化钠溶液在酒精灯上灼烧,火焰呈现黄色,显色原因是( )
| A、氯化钠受热挥发 |
| B、氯化钠受热分解 |
| C、钠离子中电子跃迁 |
| D、氯离子中电子跃迁 |
下列有机物命名正确的是( )
A、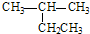 2-乙基丙烷 2-乙基丙烷 |
| B、CH3CH2CH2CH2OH 1-丁醇 |
C、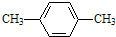 间二甲苯 间二甲苯 |
D、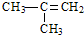 2-甲基-2-丙烯 2-甲基-2-丙烯 |
下列措施,是为了防止产生雾霾的,其中不可行的是( )
| A、停止冬季供暖,减少有害物质排放 |
| B、对锅炉和汽车等产生的有害气体和烟尘等进行处理 |
| C、退耕还林,改善生态环境 |
| D、寻找新能源,减少化石燃料的使用 |
能使干燥有色布条褪色的是( )
| A、新制氯水 | B、久置氯水 |
| C、液氯 | D、NaCl溶液 |
将1.12g铁粉加入25mL 20mol?L-1的氯化铁溶液中,充分反应后,其结果是( )
①铁有剩余,溶液呈浅绿色,Cl-浓度基本不变
②往溶液中滴入无色KSCN溶液,显红色
③Fe2+和Fe3+的物质的量之比为6:1
④氧化产物与还原产物的物质的量之比为2:5.
①铁有剩余,溶液呈浅绿色,Cl-浓度基本不变
②往溶液中滴入无色KSCN溶液,显红色
③Fe2+和Fe3+的物质的量之比为6:1
④氧化产物与还原产物的物质的量之比为2:5.
| A、①② | B、②③ | C、③④ | D、①④ |
将14g铜银合金跟足量的某浓度HNO3反应,将放出的气体与1.12LO2(标准状况)混合,通入水中,恰好全部吸收,则合金中银的质量是( )
| A、3.2g | B、10.8g |
| C、21.6g | D、5.4g |
下列反应属于吸热反应的是( )
| A、过氧化氢在MnO2催化条件下分解 |
| B、碳不完全燃烧产生CO |
| C、氢氧化钡晶体与氯化铵混合 |
| D、盐酸与氢氧化钠溶液反应 |