题目内容
15.短周期非金属元素甲~戊在元素周期表中相对位置如下表所示,下列判断不正确的是( )| 甲 | 乙 | |
| 丙 | 丁 | 戊 |
| A. | 原子半径:甲>乙 | |
| B. | 原子核外电子层数:乙<丁 | |
| C. | 原子最外层电子数:丙>丁>戊 | |
| D. | 元素的最高价氧化物对应水化物的酸性:丙<戊 |
分析 由短周期非金属元素甲~戊在元素周期表中的相对位置,可知甲为C(或N)、乙为N(或O)、丙为Si(P)、丁为P(或S)、戊为S(或Cl).
A.同周期元素原子半径从左到右逐渐减小;
B.同主族元素从下到下电子层数逐渐增多;
C.同周期元素从左到右原子最外层电子数逐渐增多;
D.元素的非金属性越强,对应的最高价氧化物对应水化物的酸性越强.
解答 解:由短周期非金属元素甲~戊在元素周期表中的相对位置,可知甲为C(或N)、乙为N(或O)、丙为Si(P)、丁为P(或S)、戊为S(或Cl).
A.同周期元素原子半径从左到右逐渐减小,故A正确;
B.同主族元素从下到下电子层数逐渐增多,故B正确;
C.同周期元素从左到右原子最外层电子数逐渐增多,故C错误;
D.非金属性戊>丙,元素的非金属性越强,对应的最高价氧化物对应水化物的酸性越强,故D正确.
故选C.
点评 本题考查元素周期表与元素周期律,为高考常见题型,侧重于学生的分析能力的考查,注意把握短周期元素元素在周期表中的位置以及元素周期率的递变规律,难度不大.

练习册系列答案
相关题目
5.下列物质转化在给定条件下能实现的是( )
| A. | Al2O3$→_{△}^{NaOH(aq)}$NaAlO2(aq)$\stackrel{CO_{2}}{→}$Al(OH)3 | |
| B. | S$\stackrel{O_{2}/点燃}{→}$SO3$\stackrel{H_{2}O}{→}$H2SO4 | |
| C. | Fe2O3$\stackrel{HCl(aq)}{→}$FeCl3(aq)$\stackrel{△}{→}$无水FeCl3 | |
| D. | NH3$\stackrel{O_{2}/催化剂}{→}$NO2$\stackrel{H_{2}O}{→}$HNO3 |
3.下列物质属于合金的是( )
| A. | 硬铝 | B. | 水银 | C. | 黄金 | D. | 金刚石 |
10.海水蕴藏着丰富的资源.下列有关海水综合利用的说法中,不正确的是( )
| A. | 从海水中可提取食盐 | B. | 海水蒸馏可得淡水 | ||
| C. | 直接电解海水可得镁 | D. | 从海水中可提取溴 |
4.下列说法中正确的是( )
| A. | 某单核粒子的核外电子排布为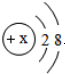 ,则该微粒一定是氖原子 ,则该微粒一定是氖原子 | |
| B. | 原子最外层只有1个电子的元素一定是金属元素 | |
| C. | NH4+与H3O+具有相同的质子数和电子数 | |
| D. | 最外层电子数是次外层电子数2倍的原子容易失去电子成为阳离子 |
18.香叶醛(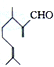 )是一种重要的香料,在硫酸的作用下能生成对异丙基甲苯(
)是一种重要的香料,在硫酸的作用下能生成对异丙基甲苯(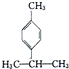 ).下列有关香叶醛与对异丙基甲苯的叙述正确的是( )
).下列有关香叶醛与对异丙基甲苯的叙述正确的是( )
 )是一种重要的香料,在硫酸的作用下能生成对异丙基甲苯(
)是一种重要的香料,在硫酸的作用下能生成对异丙基甲苯( ).下列有关香叶醛与对异丙基甲苯的叙述正确的是( )
).下列有关香叶醛与对异丙基甲苯的叙述正确的是( )| A. | 对异丙基甲苯的分子式为C10H14 | |
| B. | 香叶醛的一种同分异构体可能是芳香醇 | |
| C. | 两者互为同分异构体 | |
| D. | 两者均能与溴水反应加成反应 |