题目内容
10.海水蕴藏着丰富的资源.下列有关海水综合利用的说法中,不正确的是( )| A. | 从海水中可提取食盐 | B. | 海水蒸馏可得淡水 | ||
| C. | 直接电解海水可得镁 | D. | 从海水中可提取溴 |
分析 海水中含有丰富的资源,可以通过蒸馏获得淡水,通过蒸发获得食盐,通过氧化反应获得溴单质,但是直接电解氯化镁溶液,得到的是氯气、氢氧化镁沉淀、氧气,不会得到金属镁,据此进行解答.
解答 解:A.还是中含有大量的NaCl,可以通过蒸发还是获得食盐,故A正确;
B.海水中盐类的沸点较高,可通过蒸馏操作从而海水中获得淡水,故B正确;
C.海水中含有氯化镁,电解氯化镁溶液得到的是氯气、氢氧化镁沉淀、氧气,不会得到金属Mg,故C错误;
D.海水中含有溴元素,通过加入氧化剂,如氯气、双氧水等,可以从而海水中提取溴,故D正确;
故选C.
点评 本题考查了海水资源的综合应用,题目难度中等,涉及海水淡化、金属冶炼、海水提取溴、氯化钠等知识,试题侧重基础知识的考查,培养了学生的分析能力及灵活应用能力.

练习册系列答案
 目标测试系列答案
目标测试系列答案
相关题目
20.LiAlH4在125℃分解为LiH、H2和Al.下列说法中不正确的是( )
| A. | 乙醛在LiAlH4的作用下生成乙醇,LiAlH4作还原剂 | |
| B. | LiH中两种微粒半径:H->Li+ | |
| C. | 1mol LiAlH4在125℃完全分解,则转移4mol电子 | |
| D. | LiH溶于水的化学反应方程式:LiH+H2O═LiOH+H2↑ |
1.下列说法不正确的是( )
| A. | 常温下,向醋酸钠溶液中滴加盐酸至溶液呈中性一定有:c(CH3COOH)=c(Cl-) | |
| B. | NaHSO4溶液中滴加Ba(OH)2至溶液恰好呈中性c(Na+)>c(SO42-)>c(OH-)=c(H+) | |
| C. | 某酸式盐NaHA溶液中一定有:c(OH-)+c(A2-)=c(H+)+c(H2A) | |
| D. | 0.5 mol/L 的Na2S溶液中:$\frac{1}{2}$ c(Na+)=c(H2S)+c(HS-)+c(S2-)=0.5 mol/L |
18.在2L0.1mol•L-1 BaCl2溶液中,下列说法正确的是( )
| A. | Cl-物质的量为0.1mol | B. | Cl-物质的量浓度为0.2 mol•L-1 | ||
| C. | Ba2+物质的量为0.1mol | D. | Ba2+物质的量浓度为0.2 mol•L-1 |
5.一定条件下,乙烷发生分解反应:C2H6?C2H4+H2.一段时间后,各物质的浓度保持不变,这说明( )
| A. | 反应完全停止 | B. | 反应达到平衡状态 | ||
| C. | 反应物消耗完全 | D. | 正反应速率大于逆反应速率 |
15.短周期非金属元素甲~戊在元素周期表中相对位置如下表所示,下列判断不正确的是( )
| 甲 | 乙 | |
| 丙 | 丁 | 戊 |
| A. | 原子半径:甲>乙 | |
| B. | 原子核外电子层数:乙<丁 | |
| C. | 原子最外层电子数:丙>丁>戊 | |
| D. | 元素的最高价氧化物对应水化物的酸性:丙<戊 |
13.下列实验操作、现象和得出的结论均正确的是( )
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向25mL冷水与沸水中分别滴入5滴FeCl3饱和溶液 | 前者为黄色,后者为红褐色 | 温度升高,Fe3+的水解程度增大 |
| B | 淀粉在稀硫酸的作用下水解后,滴加NaOH溶液至碱性,再加入新制Cu(OH)2后加热 | 有砖红色沉淀生成 | 淀粉已经完全水解 |
| C | 向硝酸银溶液中滴加过量氨水 | 溶液澄清 | Ag+与NH3•H2O能大量共存 |
| D | 向饱和Na2CO3溶液中加入BaSO4固体,振荡、过滤,向滤渣中加入盐酸 | 有气体生成 | Ksp(BaCO3)>Ksp(BaSO4) |
| A. | A | B. | B | C. | C | D. | D |
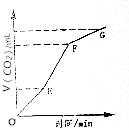 (1)下列说法中,不正确的是DEHIJ
(1)下列说法中,不正确的是DEHIJ