题目内容
 如图所示的电解池I和II中,a、b、c和d均为Pt电极.电解过程中,电极b和d上没有气体逸出,但质量均增大,且增重b<d.符合上述实验结果的盐溶液是( )
如图所示的电解池I和II中,a、b、c和d均为Pt电极.电解过程中,电极b和d上没有气体逸出,但质量均增大,且增重b<d.符合上述实验结果的盐溶液是( )| A、MgSO4,CuSO4 |
| B、AgNO3,Pb(NO3)2 |
| C、FeSO4,Al2 (SO4)3 |
| D、CuSO4,AgNO3 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:依据装置图分析电极名称a为阳极,b为阴极,c为阳极,d为阴极,结合电解原理,溶液中离子放电顺序分析判断电极反应,电极b和d上没有气体逸出,但质量均增大,说明阴极上溶液中金属离子在阴极析出金属单质,对选项分析判断.
解答:
解:装置图分析电极名称a为阳极,b为阴极,c为阳极,d为阴极,结合电解原理,溶液中离子放电顺序分析判断电极反应,电极b和d上没有气体逸出,但质量均增大,说明阴极上溶液中金属离子在阴极析出金属单质;
A、X为MgSO4,阴极电极反应为溶液中氢离子放电,无金属析出;Y为CuSO4 ,溶液中阴极上铜离子得到电子析出金属,故A错误;
B、X为AgNO3,阴极电极反应为溶液中银离子放电,电极反应为:Ag++e-=Ag,Y为Pb(NO3)2 ,阴极上溶液中氢离子放电,无金属析出,故B错误;
C、X为FeSO4,阴极是溶液中氢离子得到电子生成氢气,无金属析出,Y为Al2 (SO4)3,阴极上是氢离子放电无金属析出,故C错误;
D、X为CuSO4,阴极是溶液中铜离子析出,电极反应Cu2++2e-=Cu,Y为AgNO3,阴极电极反应为溶液中银离子放电,电极反应为:Ag++e-=Ag,依据电子守恒Cu~2Ag,增重d>b,符合题意,故D正确.
故选D.
A、X为MgSO4,阴极电极反应为溶液中氢离子放电,无金属析出;Y为CuSO4 ,溶液中阴极上铜离子得到电子析出金属,故A错误;
B、X为AgNO3,阴极电极反应为溶液中银离子放电,电极反应为:Ag++e-=Ag,Y为Pb(NO3)2 ,阴极上溶液中氢离子放电,无金属析出,故B错误;
C、X为FeSO4,阴极是溶液中氢离子得到电子生成氢气,无金属析出,Y为Al2 (SO4)3,阴极上是氢离子放电无金属析出,故C错误;
D、X为CuSO4,阴极是溶液中铜离子析出,电极反应Cu2++2e-=Cu,Y为AgNO3,阴极电极反应为溶液中银离子放电,电极反应为:Ag++e-=Ag,依据电子守恒Cu~2Ag,增重d>b,符合题意,故D正确.
故选D.
点评:本题考查了电解原理的分析应用,主要是电极反应,溶液中离子浓度放电顺序的判断,电极反应书写方法和电子守恒的计算应用,掌握基础是关键,题目难度中等.

练习册系列答案
 能力评价系列答案
能力评价系列答案 唐印文化课时测评系列答案
唐印文化课时测评系列答案 导学与测试系列答案
导学与测试系列答案
相关题目
下列烷烃的一氯取代物中没有同分异构体的是( )
| A、2-甲基丙烷 | B、丙烷 |
| C、甲烷 | D、乙烷 |
室温下,对于0.10mol?L-1的氨水,下列判断正确的是( )
| A、用相同浓度的HNO3溶液中和,硝酸体积小于氨水时,溶液可能呈中性 |
| B、温度不变,加水稀释后溶液中c(NH4+)?c(OH-)不变 |
| C、加水稀释后,溶液中导电粒子的数目减少 |
| D、其溶液的pH=13 |
下列离子方程式书写正确的是( )
| A、向AlCl3溶液中加入过量的浓氨水:Al3++4NH3?H2O═AlO2-+4NH4++2H2O |
| B、往CaCl2溶液通入少量的CO2:Ca2++CO2+H2O═CaCO3↓+2H+ |
| C、碳酸氢铵溶液中加入过量氢氧化钠溶液:HCO3-+OH-═CO32-+H2O |
| D、向Ba(OH)2溶液中加入少量的NaHSO3溶液:HSO3-+Ba2++OH-═BaSO3↓+H2O |
空间实验室“天宫一号”的供电系统中有再生氢氧燃料电池(RFC),RFC是一种将水电解技术与氢氧燃料电池技术相结合的可充电电池,工作原理如图如示.下列有关说法正确的是( )

| A、当有0.2 mol电子转移时,a电极产生2.24 L H2 |
| B、b电极上发生的电极反应式为2H++2e-═H2↑ |
| C、d电极上发生的电极反应式为O2+4H++4e-═2H2O |
| D、d电极上进行氧化反应,B池中的H+可以通过隔膜进入A池 |
下列各图示实验设计和操作合理的是( )
A、 证明非金属性强弱:S>C>Si |
B、 制备少量氧气 |
C、 配制一定物质的量浓度的硫酸溶液 |
D、 制备少量乙酸丁酯 |
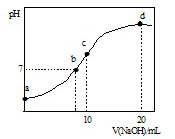 常温下,向20.00mL 0.1000mol?L-1 (NH4)2SO4溶液中逐滴加入0.2000mol?L-1 NaOH时,溶液的pH与所加NaOH溶液体积的关系如右图所示(不考虑挥发).下列说法正确的是 ( )
常温下,向20.00mL 0.1000mol?L-1 (NH4)2SO4溶液中逐滴加入0.2000mol?L-1 NaOH时,溶液的pH与所加NaOH溶液体积的关系如右图所示(不考虑挥发).下列说法正确的是 ( )| A、点a所示溶液中:c(NH4+)>c(SO42-)>c(OH-)>c(H+) |
| B、点b所示溶液中:c(NH4+)=c(Na+)>c(H+)=c(OH-) |
| C、点c所示溶液中:c(SO42-)+c(H+)=c(NH3?H2O )+c(OH-) |
| D、点d所示溶液中:c(SO42-)>c(NH3?H2O )>c(OH-)>c(NH4+) |
 光气 (COCl2)在塑料、制革、制药等工业中有许多用途,工业上采用高温下CO与Cl2在活性炭催化下合成.
光气 (COCl2)在塑料、制革、制药等工业中有许多用途,工业上采用高温下CO与Cl2在活性炭催化下合成.