题目内容
16. 氮及其化合物在工农业生产生活中应用广泛,请解决下列问题.
氮及其化合物在工农业生产生活中应用广泛,请解决下列问题.(1)硫酸铜溶液时白磷引起中毒的一种解毒剂:
P4+CuSO4+H2O→Cu3P+H3PO4+H2SO4,若6molH3PO4生成,则被CuSO4氧化的P4的物质的量为0.75mol.
(2)氮的化合物合成、应用及氮的固定一直是科学研究的热点.以CO2与NH3为原料合成化肥尿素的主要反应如下:
①2NH3(g)+CO2(g)=NH2CO2NH4(s);△H=-159.47kJ•mol-1
②NH2CO2NH4(s)=CO (NH2)2(s)+H2O(g);△H=a kJ•mol-1
③2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(g);△H=-86.98kJ•mol-1
则a为+72.49.
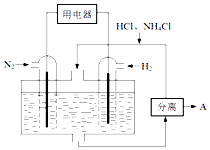
(3)如图表示使用新型电极材料,以N2、H2为电极反应物,以HCl-NH4Cl为电解质溶液制造出既能提供能量,同时又能实现氮固定的新型燃料电池.请写出该电池的正极反应式N2+6e-+8H+=2NH4+.生产中可分离出的物质A的化学式为NH4Cl.
(4)常温下,向0.1mol/L氨水中加入少许N2O5,使溶液中c(NH3•H2O):c(NH4+)=5:9,此时溶液的
pH=9.(25℃时,NH3•H2O的电离常数Kb=1.8×10-5)
(5)SiO2溶于氢氟酸后生成一种极强的二元酸和水,经分析该酸由3种元素组成,其中氟严肃的质量分数为79.17%.请写出SiO2溶于氢氟酸的离子方程式SiO2+6HF=2H++SiF62-+2H2O.
分析 (1)Cu元素的化合价由+2价降低到+1价,CuSO4是氧化剂,P4中部分磷元素由0价降低到-3价,部分磷元素由0价升高到+5价,磷元素的化合价既升高又降低,所以P4既是氧化剂又是还原剂,根据电子转移是计算被CuSO4氧化的P4的物质的量;
(2)①2NH3(g)+CO2(g)=NH2CO2NH4(s);△H=-159.47kJ•mol-1
②NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g);△H=a kJ•mol-1
③2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(g);△H=-86.98kJ•mol-1
依据热化学方程式和盖斯定律①+②=③,依据热化学方程式和盖斯定律来计算;
(3)原电池正极发生还原反应,依据装置图分析判断分离出氯化铵;
(4)常温下,向0.1mol/L氨水中加入少许N2O5,五氧化二氮和水反应生成硝酸,硝酸和氨水反应,溶液中c(NH3•H2O):c(NH4+)=5:9,溶液中溶质为硝酸铵和一水合氨,根据NH3•H2O的电离平衡常数计算;
(5)依据所给质量分数求算该酸的化学式,然后书写即可.
解答 解:(1)Cu元素的化合价由+2价降低到+1价,CuSO4是氧化剂,P4中部分磷元素由0价降低到-3价,部分磷元素由0价升高到+5价,磷元素的化合价既升高又降低,所以P4既是氧化剂又是还原剂,若6molH3PO4生成,则参加反应CuSO4为6mol×$\frac{60}{24}$=15mol,根据电子转移守恒,被CuSO4氧化的P4的物质的量为$\frac{15mol×1}{4×5}$=0.75mol,
故答案为:0.75mol;
(2)①2NH3(g)+CO2(g)=NH2CO2NH4(s);△H=-159.47kJ•mol-1
②NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g);△H=a kJ•mol-1
③2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(g);△H=-86.98kJ•mol-1
依据热化学方程式和盖斯定律①+②=③,得到-159.47KJ/mol+a=-86.98KJ/mol
a=+72.49KJ/mol;
故答案为:+72.49;
(3)以N2、H2为原料,以HCl-NH4Cl为电解质溶液构成新型燃料电池,正极发生还原反应,即氮气被还原生成NH4+,电极反应式为N2+6e-+8H+=2NH4+;负极是氢气失电子生成氢离子,政绩生成铵根离子在电解质溶液中可以分离出氯化铵;
故答案为:N2+6e-+8H+=2NH4+; NH4Cl;
(4)常温下,向0.1mol/L氨水中加入少许N2O5,五氧化二氮和0.1水反应生成硝酸,硝酸和氨水反应,溶液中c(NH3•H2O):c(NH4+)=5:9,溶液中溶质为硝酸铵和一水合氨,NH3•H2O?NH4++OH-,25℃时.NH3•H2O的电离平衡常数Kb=1.8×10-5=$\frac{c(O{H}^{-})×\frac{9}{14}×0.1}{\frac{5}{14}×0.1}$,c(OH-)=10-5mol/L,c(H+)=10-9mol/L,PH=9,
故答案为:9;
(5)SiO2溶于氢氟酸后生成一种极强的二元酸和水,该酸由3种元素组成,其中氟元素的质量分数为79.17%,分子中H原子数目为2,令该酸的化学式为:H2SixFy,根据化合价代数和为0可知2+4x-y=0,由氟元素质量分数有$\frac{19y}{2+28x+19y}$×100%=79.17%,联立解得x=1,y=6,故该酸为H2SiF6,故SiO2溶于氢氟酸的离子反应方程式为:SiO2+6HF=2H++SiF62-+2H2O,故答案为:SiO2+6HF=2H++SiF62-+2H2O.
点评 本题考查热化学方程式书写方法和盖斯定律计算应用,图象分析和反应条件判断,信息应用能力,原电池电极反应书写的方法应用,题目难度较大.

(1)用电弧法合成的储氢纳米碳管常伴有大量的碳纳米颗粒(杂质),这种颗粒可用如下氧化法提纯,请完成该反应的化学方程式:
5C+4KMnO4+6H2SO4=5CO2↑+4MnSO4+2K2SO4+6H2O
(2)在2L密闭容器中加入NO和活性炭(无杂质),生成气体E和F.当温度分别在T1和T2时,测得各物质平衡时物质的量如表:
| n/mol T/℃ | 活性炭 | NO | E | F |
| 初始 | 2.030 | 0.100 | 0 | 0 |
| T1 | 2.000 | 0.040 | 0.030 | 0.030 |
| T2 | 2.005 | 0.050 | 0.025 | 0.025 |
①计算:K1=$\frac{9}{16}$.
②根据上述信息判断,温度T1和T2的关系是(填序号)C.
A. T1>T2 B. T1<T2 C.无法比较
(3)工业上利用CO和水蒸气在一定条件下发生反应制取氢气:CO(g)+H2O(g)?CO2(g)+H2(g);△H=-41kJ/mol
已知:2H2O (g)═2H2(g)+O2(g);△H=+484kJ/mol,
①写出CO完全燃烧生成CO2的热化学方程式:2CO(g)+O2(g)═2CO2(g)△H=-566 kJ/mol.
②某温度下,在一容积可变的容器中,CO转化生成CO2的反应达到平衡时,CO、O2和CO2的物质的量分别为4mol、2mol、和4mol.保持温度和压强不变,对平衡混合物中三者的物质的量作如下调整,可使平衡右移的是:(填序号)A.
A. 均增加1mol B. 均加倍 C. 均减少1mol D. 均减半.
| A. | 8.67---9.26 | B. | 7.00 | C. | 7.35---7.45 | D. | 大于5.70 |
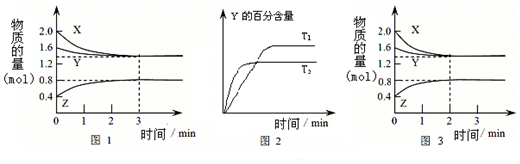
| A. | 容器中发生的反应可表示为:2X(g)+Y(g)?2Z(g) | |
| B. | 0~3 min内,v(X)=0.2 mol•L-1•min-1 | |
| C. | 其他条件不变升高温度,v正、v逆都增大,且重新平衡前v正>v逆 | |
| D. | 若改变条件,使反应进程如图3所示,则改变的条件可能是增大压强 |
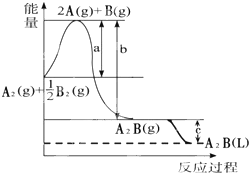 已知:A2(g)+$\frac{1}{2}$B2(g)═A2B(g),反应过程中能量变化如图,问:
已知:A2(g)+$\frac{1}{2}$B2(g)═A2B(g),反应过程中能量变化如图,问: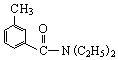 ; DEET在一定条件下,可通过下面的路线来合成:
; DEET在一定条件下,可通过下面的路线来合成: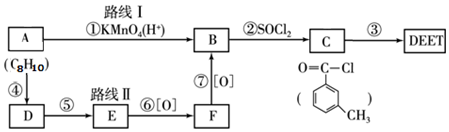
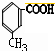 .
.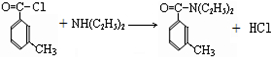 .
. .
. 某无色溶液中含有K+、Cl-、OH-、SO32-、SO42-,为检验溶液中所含的某些阴离子,限用的试剂有:盐酸、硝酸、硝酸银溶液、硝酸钡溶液、溴水和酚酞溶液.检验其中OH-的实验方法省略,检验其他阴离子的过程如图所示.
某无色溶液中含有K+、Cl-、OH-、SO32-、SO42-,为检验溶液中所含的某些阴离子,限用的试剂有:盐酸、硝酸、硝酸银溶液、硝酸钡溶液、溴水和酚酞溶液.检验其中OH-的实验方法省略,检验其他阴离子的过程如图所示.