题目内容
16.在密闭容器中充入4molHI,在一定温度下2HI(g)?H2(g)+I2(g)达到平衡时,有30%的HI发生分解,则平衡时混合气体总的物质的量是( )| A. | 4 mol | B. | 3 mol | C. | 2.5mol | D. | 1.2 mol |
分析 可逆反应2HI(g)?H2(g)+I2(g)中,反应前后气体的体积相等,则反应过程中气体总物质的量始终不变,据此进行解答.
解答 解:2HI(g)?H2(g)+I2(g)为气体体积不变的反应,则反应过程中气体的总物质的量始终不变,
所以平衡时气体总物质的量仍然为4mol,
故选A.
点评 本题考查了化学平衡的计算,题目难度不大,明确该反应前后气体体积不变为解答关键,试题侧重基础知识的考查,培养了学生的分析能力及灵活应用能力.

练习册系列答案
 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案
相关题目
6.下列离子方程式书写正确的是( )
| A. | 醋酸溶液与水垢中的CaCO3反应:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| B. | 用稀硝酸洗涤试管内壁的银镜:Ag+2H++NO3-═Ag++NO↑+H2O | |
| C. | Ca(HCO3)2溶液与少量NaOH溶液反应:Ca2++HCO3-+OH-═CaCO3↓+H2O | |
| D. | 明矾溶于水产生Al(OH)3胶体:Al3++3H2O═Al(OH)3↓+3H+ |
7.下列叙述正确的是( )
| A. | 凡吸热反应均需在加热条件下才能发生 | |
| B. | 离子化合物中不可能含有共价键 | |
| C. | 液氨作为清洁能源的反应原理是4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O | |
| D. | 实验收集NO和乙烯常用排水法不能用排空气法 |
4.下列各有机物的数目与分子式为C4H7ClO2且能与NaHCO3溶液反应生成CO2的有机物的数目(不考虑立体异构)相同的是( )
| A. | 甲苯的一氯代物 | B. | 分子式为C5H10的烯烃 | ||
| C. | 相对分子质量为74的一元醇 | D. | 立方烷( )的二硝基取代物 )的二硝基取代物 |
11.下列各组离子在水溶液中能大量共存的是( )
| A. | Na+、SO42-、Cu2+、Cl- | B. | Fe2+、Na+、OH-、K+ | ||
| C. | K+、CO32-、Cl-、Ag+ | D. | H+、Cl-、Na+、CO32- |
6.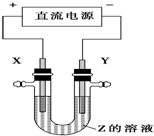 利用如图所示装置,当X、Y选用不同材料时,可将电解原理广泛应用于工业生产.下列说法中正确的是( )
利用如图所示装置,当X、Y选用不同材料时,可将电解原理广泛应用于工业生产.下列说法中正确的是( )
 利用如图所示装置,当X、Y选用不同材料时,可将电解原理广泛应用于工业生产.下列说法中正确的是( )
利用如图所示装置,当X、Y选用不同材料时,可将电解原理广泛应用于工业生产.下列说法中正确的是( )| A. | 氯碱工业中,X、Y均为石墨,X附近能得到氢氧化钠 | |
| B. | 铜的精炼中,X是纯铜,Y是粗铜,Z是CuSO4 | |
| C. | 在铁片上镀铜时,Y是纯铜 | |
| D. | 外加电流的阴极保护法中,Y是待保护金属 |