题目内容
将一定质量的镁铝合金投入200mL一定浓度的盐酸中,合金完全溶解.向所得溶液中滴加浓度为4mol/L的NaOH溶液,生成的沉淀跟加入的NaOH溶液的体积关系如下图.(横坐标体积单位是mL,纵坐标质量单位是g)(需要写出简单的求解步骤)
求:(1)写出镁与盐酸反应的化学方程式并用双线桥标出转移的电子数目
(2)所用HCl的物质的量浓度;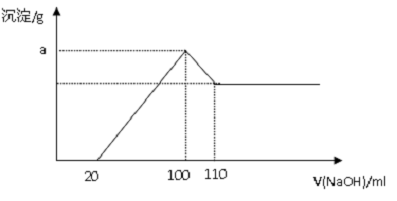
(3)计算沉淀最大量a 的值.
求:(1)写出镁与盐酸反应的化学方程式并用双线桥标出转移的电子数目
(2)所用HCl的物质的量浓度;

(3)计算沉淀最大量a 的值.
考点:镁、铝的重要化合物
专题:
分析:(1)镁与盐酸反应生成氯化镁和氢气;
(2)加入氢氧化钠溶液为100mL时,沉淀量最大,此时为Mg(OH)2和Al(OH)3,溶液为氯化钠溶液,根据钠元素守恒此时溶液中n(NaCl)=n(NaOH),据此计算出n(HCl),再利用c=
计算盐酸的物质的量浓度.
(3)a的值是当沉淀量达到最大值的质量值,根据①②的过程②进行计算即可.
(2)加入氢氧化钠溶液为100mL时,沉淀量最大,此时为Mg(OH)2和Al(OH)3,溶液为氯化钠溶液,根据钠元素守恒此时溶液中n(NaCl)=n(NaOH),据此计算出n(HCl),再利用c=
| n |
| V |
(3)a的值是当沉淀量达到最大值的质量值,根据①②的过程②进行计算即可.
解答:
解:(1)镁与盐酸反应生成氯化镁和氢气,反应中镁失电子,氢得到电子生成氢气,双线桥表示的氧化还原反应为: ,故答案为:
,故答案为: ;
;
(2)当沉淀为a g时,溶液中溶质成分只有NaCl,故而根据原子守恒可得:
n(HCl)=n(NaCl)=n(NaOH)=4mol/L×0.1L=0.4mol
所以c(HCl)=
=2mol/L
答:所用HCl的物质的量浓度为2mol/L;
(3)由题意可知:
Al(OH)3+OH-=AlO2-+2H2O
1 1
n 4mol/L×0.01L
得:n[Al(OH)3]=0.04mol
m[Al(OH)3]=3.12g
Mg2++2OH-═Mg(OH)2↓
2 1
4mol/L×0.05 n
得:n[Mg(OH)2]=0.1mol
m[Mg(OH)2]=5.8g
a=3.12+5.8=8.92g
答:a的值为 8.92g.
 ,故答案为:
,故答案为: ;
;(2)当沉淀为a g时,溶液中溶质成分只有NaCl,故而根据原子守恒可得:
n(HCl)=n(NaCl)=n(NaOH)=4mol/L×0.1L=0.4mol
所以c(HCl)=
| 0.4mol |
| 0.2L |
答:所用HCl的物质的量浓度为2mol/L;
(3)由题意可知:
Al(OH)3+OH-=AlO2-+2H2O
1 1
n 4mol/L×0.01L
得:n[Al(OH)3]=0.04mol
m[Al(OH)3]=3.12g
Mg2++2OH-═Mg(OH)2↓
2 1
4mol/L×0.05 n
得:n[Mg(OH)2]=0.1mol
m[Mg(OH)2]=5.8g
a=3.12+5.8=8.92g
答:a的值为 8.92g.
点评:本题考查镁铝化合物性质、混合物的计算,以图象题的形式考查,题目难度中等,分析图象各阶段的发生的反应是解题关键,再利用守恒计算.

练习册系列答案
相关题目
下列有关物质性质的应用错误的是( )
| A、二氧化硅不与强酸反应,可用石英玻璃容器盛放氢氟酸 |
| B、碳酸氢钠具有弱酸性,可用于食品发酵 |
| C、次氯酸钠具有强氧化性,可用于配制消毒液 |
| D、明矾能水解生成Al(OH)3胶体,可用作净水剂 |
用已知浓度的盐酸滴定未知浓度的NaOH溶液(NaOH溶液放于锥形瓶中),选酚酞作指示剂,下列操作会导致测定结果偏低的是( )
| A、酸式滴定管未润洗就装标准液滴定 |
| B、读取标准液读数时,滴定前平视,滴定到终点后俯视 |
| C、滴定前酸式滴定管尖嘴处有气泡未排除,滴定后气泡消失 |
| D、滴定达终点时发现滴定管尖嘴处挂着一滴液滴 |
化学与人类生活、社会可持续发展密切相关.下列说法正确的是( )
| A、漂白粉的有效成分是Ca(ClO)2和CaCl2 |
| B、为消除碘缺乏病,我国政府规定在生产食用盐时必须加入一定量的单质碘 |
| C、向豆浆中加入盐卤可以做豆腐 |
| D、SO2的大量排放带来的环境问题是光化学烟雾和酸雨 |
常温下,下列各组离子在指定溶液中能大量共存的是( )
| A、pH=1的溶液中:Fe2+、NO3-、SO42-、Na+ | ||
| B、由水电离的C(H+)=1×10-14mol?L-1的溶液中:Ca2+、K+、Cl-、HCO3- | ||
C、
| ||
| D、c(Fe3+)=0.1mol?L-1的溶液中:K+、SO42-、CO32-、Cl- |
恒温条件下,将NO2装入带活塞的密闭容器中,当反应2NO2(g)?N2O4(g)达到平衡后,慢慢压缩气体体积,下列叙述正确的是( )
| A、若体积减小一半,则压强为原来的两倍 |
| B、平衡向右移动,混合气体颜色一定会变浅 |
| C、若体积减小一半,压强增大,但小于原来的两倍 |
| D、平衡向右移动,混合气体密度减小 |
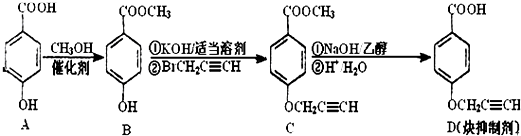
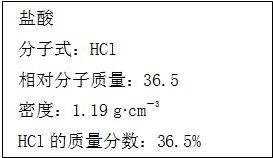 如图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:
如图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题: