题目内容
11.石油被称为“工业的血液”,以石油为原料不仅可以得到各种燃料油,还可以获得多种有机化工原料.请回答下列问题:(1)将石蜡油与碎瓷片混合共热,产生的混合气体冷却至室温后,其成分如下:
| 物质 | CH4 | CH3-CH3 | CH2═CH2 |
| 物质的量分数 | 20% | 30% | 50% |
(2)经发现,石蜡油与碎瓷片混合共热的产物中,除气态烃CH4、C2H6、CH2═CH2外,还有另一种液态烃M生成.0.2mol该液态烃在O2中完全燃烧时,得到的两种生成物的物质的量均为1.2mol.
①烃M的分子式为C6H12.
②烃N是烃M的一种同分异构体,其结构中含有4个甲基,则烃N的结构简式为
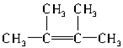 .
.③烃N中一定处于同一平面的碳原子数为6.
④写出烃N发生自身加聚反应的化学方程式
 .
.
分析 (1)已知混合气体为2mol,其中乙烯为50%,则乙烯为1mol,根据反应方程式计算消耗的溴;
(2)根据原子守恒计算烃分子中N(C)、N(H),进而确定烃的分子式;根据乙烯的分子结构可知与C=C相连的原子在一个平面内,要保证6个碳原子在一个平面内,则另外4个碳必须直接与C=C相连,由此分析解答.
解答 解:(1)已知混合气体为2mol,其中乙烯为50%,则乙烯为1mol,乙烯与溴反应的方程式为CH2=CH2+Br2→CH2Br-CH2Br,则消耗Br2的物质的量为1mol;
故答案为:1mol;
(2)完全燃烧0.2mol某烃,得到的两种生成物的物质的量均为1.2mol,则生成1.2molCO2和1.2molH2O,
故烃分子中N(C)=$\frac{1.2mol×1}{0.2mol}$=6,N(H)=$\frac{1.2mol×2}{0.2mol}$=12,
①所以该烃的分子式是C6H12,故答案为:C6H12;
②根据乙烯的分子结构可知与C=C相连的原子在一个平面内,要保证6个碳原子在一个平面内,则另外4个碳必须直接与C=C相连,结构简式为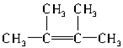 ,故答案为:
,故答案为: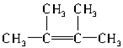 ;
;
③乙烯是平面结构,乙烯中的4个氢原子和2个碳原子共平面,由于有机物可以看做是用4个甲基取代了乙烯中的4个H原子,故此有机物中的这6个碳原子一定共平面,故答案为:6;
④2,3-二甲基-2-丁烯可发生加聚反应,反应方程式为: ,
,
故答案为: .
.
点评 本题考查有机物分子式的确定、同分异构体,题目比较基础,注意掌握燃烧法利用原子守恒确定分子式以及原子共面的判断方法.

练习册系列答案
相关题目
1.在2L的恒容密闭容器中充入2mol SO2和1mol O2,发生反应:2SO2(g)+O2(g)?2SO3(g),下列有关说法正确的是( )
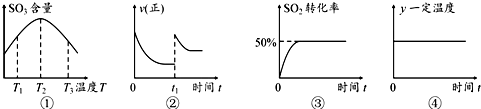

| A. | 由图①可知:该反应的△H>0 | |
| B. | 在图②中的t1时充入少量氩气,容器内压强增大,平衡右移 | |
| C. | 图③所示条件下,平衡常数为2 | |
| D. | 图④中的y可以表示平衡常数或密度 |
2.常温常压下,某烧碱溶液与0.05mol氯气恰好完全反应,得到pH=9的混合溶液(溶质为NaCl与NaClO).下列说法正确的是(NA代表阿伏伽德罗常数)( )
| A. | 氯气的体积为1.12 L | |
| B. | 原烧碱溶液中含溶质离子0.2NA个 | |
| C. | 所得溶液中含OH-的数目为1×10-5NA | |
| D. | 所得溶液中ClO-的数目为0.05NA |
19.下列说法正确的是( )
| A. | 基态时,相同周期的两种元素原子所含的能级和能层是一样的 | |
| B. | 基态时,稀有气体元素原子的价层电子数都为8 | |
| C. | 基态时,同种元素的原子和离子的轨道排布式一样 | |
| D. | 非金属元素原子的d轨道一定不填充电子或填满电子 |
16.有关糖类叙述正确的是( )
| A. | 糖类是有甜的有机物 | |
| B. | 糖类物质又叫碳水化合物,因此所有的糖类均可用通式Cn(H2O)m来表示 | |
| C. | 糖类物质和碳水化合物没有实质的联系 | |
| D. | 糖类可以分为单糖和多糖 |
3.O2F2可以发生反应:H2S+4O2F2→SF6+2HF+4O2,下列说法正确的是( )
| A. | 氧气是氧化产物 | |
| B. | O2F2既是氧化剂又是还原剂 | |
| C. | 若生成4.48 L HF,则转移0.8 mol电子 | |
| D. | 还原剂与氧化剂的物质的量之比为1:4 |
4.下列反应的离子方程式中不正确的是( )
| A. | 碳酸钙中滴入盐酸 CaCO3+2H+═Ca2++CO2↑+H2O | |
| B. | Fe(OH)3 中滴入硫酸 OH-+H +═H2O | |
| C. | AgNO3中滴入NaCl溶液 Ag ++Cl-═AgCl↓ | |
| D. | CO2通入到足量NaOH溶液中CO2+2OH-═CO32-+H2O |