题目内容
18.工业上常用铁制容器盛装冷的浓硫酸.为研究铁制材料与热的浓硫酸的反应,某学习小组进行了以下探究活动.【探究一】
(1)将已除去表面氧化物的铁钉(碳素钢)放入冷的浓硫酸中,10min后投入硫酸铜溶液中,片刻后取出观察,铁钉表面无明显变化,其原因是铁钉表面被钝化.
(2)另称取铁钉6.0g放入15.0mL浓硫酸中,加热,充分反应后得到溶液X并收集到气体Y.
①甲同学认为X中除Fe3+外还可能含有Fe2+.若要确认其中是否含有Fe2+,应选用d(填序号).
a.KSCN溶液和新制氯水
b.铁粉和KSCN溶液
c.浓氨水
d.酸性KMnO4溶液
②乙同学取336mL(标准状况)气体Y通入足量溴水中,发生反应:SO2+Br2+2H2O═2HBr+H2SO4,然后加入足量BaCl2溶液,经适当操作后,得2.33g干燥固体.由此推知气体Y中SO2的体积分数为66.7%.
【探究二】
分析上述实验中所得SO2的体积分数,丙同学认为气体Y中还可能含有H2和Q气体.为此设计了如图所示的探究实验装置(图中夹持仪器已省略).

(3)装置B中试剂的作用是检验SO2是否除尽.
(4)认为气体Y中还可能含有Q的理由是C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O
(用化学方程式表示).
(5)为确认Q的存在,需添加装置M于c(填序号).
a.装置A之前 b.装置A、B间
c.装置B、C间 d.装置C、D间
(6)如果气体Y中含有H2,实验现象应是装置D中固体由黑色变为红色,装置E中的无水硫酸铜变为蓝色.
分析 (1)常温下,铁和浓硫酸发生钝化现象;
(2)①亚铁离子具有还原性,能被酸性高锰酸钾溶液氧化而使酸性高锰酸钾溶液褪色;
②根据SO2+Br2+2H2O═2HBr+H2SO4知,二氧化硫被氧化生成硫酸,硫酸和氯化钡反应生成硫酸钡沉淀,所以2.33g沉淀是BaSO4,n(BaSO4)=$\frac{2.33g}{233g/mol}$=0.01mol,根据S原子守恒得n(BaSO4)=n(S)=n(SO2)=0.01mol,标况下二氧化硫体积=0.01mol×22.4L/mol=224mL;
(3)品红溶液能检验二氧化硫存在;
(4)Q为CO2,是碳和浓硫酸加热反应生成;
(5)碳和浓硫酸反应生成二氧化碳,所以Q为CO2,二氧化硫和二氧化碳都能使澄清石灰水变浑浊,所以应该在排除二氧化硫条件下将气体通入澄清石灰水中检验二氧化碳;
(6)氢气具有还原性,在加热条件下,能将黑色的CuO还原为红色的Cu,且生成水,水能使无水硫酸铜变蓝色.
解答 解:(1)常温下,铁和浓硫酸反应生成一层致密的氧化物薄膜而阻止进一步被氧化,该现象为钝化现象,所以将铁钉放入浓硫酸片刻无明显变化的原因是铁钉表面被钝化,故答案为:铁钉表面被钝化;
(2)①a.氯水能将亚铁离子氧化为铁离子,铁离子和KSCN溶液反应导致溶液呈血红色,但不能确定原来溶液中一定含有亚铁离子,故a错误;
b.铁粉和酸反应生成亚铁离子,不能确定原来溶液中是否含有亚铁离子,故b错误;
c.浓氨水和亚铁离子反应生成氢氧化亚铁沉淀,氢氧化亚铁能被氧化生成氢氧化铁红褐色沉淀,不能确定溶液中一定含有亚铁离子,故c错误;
d.亚铁离子具有还原性,能被酸性高锰酸钾溶液氧化而使酸性高锰酸钾溶液褪色,所以可以用酸性高锰酸钾溶液检验亚铁离子,故d正确;
故选d;
②根据SO2+Br2+2H2O═2HBr+H2SO4知,二氧化硫被氧化生成硫酸,硫酸和氯化钡反应生成硫酸钡沉淀,所以2.33g沉淀是BaSO4,n(BaSO4)=$\frac{2.33g}{233g/mol}$=0.01mol,根据S原子守恒得n(BaSO4)=n(S)=n(SO2)=0.01mol,标况下二氧化硫体积=0.01mol×22.4L/mol=224mL,二氧化硫体积分数=$\frac{224ml}{336ml}$×100%=66.7%,
故答案为:66.7%;
(3)品红溶液能检验二氧化硫存在,所以该装置的作用是检验SO2是否除尽,故答案为:检验SO2是否除尽;
(4)气体Y中还可能含有Q的理由是碳和浓硫酸加热反应生成,反应的化学方程式为:C+2H2SO4(浓) $\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O,
故答案为:C+2H2SO4(浓) $\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O;
(5)碳和浓硫酸反应生成二氧化碳,所以Q为CO2,二氧化硫和二氧化碳都能使澄清石灰水变浑浊,所以应该在排除二氧化硫条件下将气体通入澄清石灰水中检验二氧化碳,故选c,
故答案为:c;
(6)氢气具有还原性,在加热条件下,能将黑色的CuO还原为红色的Cu,且生成水,水能使无水硫酸铜变蓝色,所以如果Y中含有氢气,预计实验现象是D中固体由黑变红,E中固体由白变蓝,故答案为:装置D中固体由黑色变为红色,装置E中的无水硫酸铜变为蓝色.
点评 本题考查性质实验方案评价,为高频考点,明确实验原理是解本题关键,知道每个装置可能发生的反应及其作用,难点是判断碱石灰作用,题目难度中等.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| A. | 等浓度NaHSO4和Ba(OH)2两溶液等体积混合H++SO42-+Ba2++OH-═BaSO4↓+H2O | |
| B. | 在含有Mn2+的溶液中加入稀硝酸酸化,再加入PbO2反应体系显紫红色5PbO2+2Mn2++4H+═5Pb2++2MnO4-+2H2O | |
| C. | 硫酸亚铁溶液中加入过氧化氢溶液:2Fe2++H2O2+2H+═2Fe3++2H2O | |
| D. | Na2O2投入H218O中:2H218O+2Na2O2═4Na++4OH-+18O2↑ |
| A. | 若X、Y原子序数相差l,Y为IIA族,则X一定是IIIA族 | |
| B. | 若Y(OH)m易溶于水,则X(OH)n一定不溶于水 | |
| C. | 若HnXOm为强酸,则X的氢化物溶液于水一定显酸性 | |
| D. | 若Y元素形成的单质是气体,则X元素形成的单质一定也是气体 |
| A. | 升高温度,对正反应的反应速率影响更大 | |
| B. | 增大压强,对正反应的反应速率影响更大 | |
| C. | 减小反应物浓度,对逆反应的反应速率影响更大 | |
| D. | 加入催化剂,同等程度地改变正、逆反反应速率 |
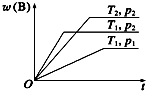 可逆反应:aA(g)+bB(g)?cC(g)在不同温度(T1和T2)及压强(p1和p2)下混合气体中B的质量分数w(B)与反应时间(t)的关系如图所示.下列判断正确的是( )
可逆反应:aA(g)+bB(g)?cC(g)在不同温度(T1和T2)及压强(p1和p2)下混合气体中B的质量分数w(B)与反应时间(t)的关系如图所示.下列判断正确的是( )| A. | a+b<c,正反应为放热反应 | B. | a+b<c,正反应为吸热反应 | ||
| C. | a+b>c,正反应为吸热反应 | D. | a+b>c,正反应为放热反应 |
| A. | K=$\frac{[N{H}_{3}][HCl]}{[N{H}_{4}Cl]}$ | B. | K=$\frac{[N{H}_{4}Cl]}{[N{H}_{3}][HCl]}$ | C. | K=[NH3][HCl] | D. | K=$\frac{[N{H}_{3}]}{[N{H}_{4}Cl]}$ |
| A. | 酒精和水 | B. | 溴苯和水 | C. | 甘油和水 | D. | 苯和酒精 |