题目内容
11.A是一种常见的气态烃,其中C、H元素质量比为6:1,其标准状况下的密度为1.25g•L-1.B、C、D都是含有C、H、O三种元素的有机物,其中D是一种常见厨房调味品中的主要成分.A、B、C、D间有如下转化关系: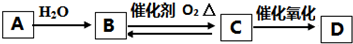
请回答下列问题:
(1)D物质中的官能团羧基.(写名称)
(2)A→B的反应类型加成反应.
(3)B→C的反应方程式2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O.
分析 A是一种常见的气态烃,其中C、H元素质量比为6:1,其标准状况下的密度为1.25g•L-1.M=1.25g/L×22.4L/mol=28g/mol,C、H原子个数比为$\frac{6}{12}$:$\frac{1}{1}$=1:2,设分子式为(CH2)n,由14×n=28,解得n=2,即A为CH2=CH2,结合转化关系可知,A与水发生加成反应生成B为CH3CH2OH,B发生催化氧化生成C为CH3CHO,D为CH3COOH,以此来解答.
解答 解:A是一种常见的气态烃,其中C、H元素质量比为6:1,其标准状况下的密度为1.25g•L-1.M=1.25g/L×22.4L/mol=28g/mol,C、H原子个数比为$\frac{6}{12}$:$\frac{1}{1}$=1:2,设分子式为(CH2)n,由14×n=28,解得n=2,即A为CH2=CH2,结合转化关系可知,A与水发生加成反应生成B为CH3CH2OH,B发生催化氧化生成C为CH3CHO,D为CH3COOH,
(1)D中官能团为羧基,故答案为:羧基;
(2)A→B的反应类型为加成反应,故答案为:加成反应;
(3)B→C的反应方程式为2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O,故答案为:2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O.
点评 本题考查有机物的推断,为高频考点,把握乙烯的分子式确定为推断的关键为解答的关键,侧重分析与推断能力的考查,注意有机物结构与性质、有机反应的应用,题目难度不大.

练习册系列答案
相关题目
1.月球的土壤中含有丰富的可控核聚变燃料3He,月球玄武岩中蕴藏着丰富的钛、铁、铬、镍、钠、镁、硅、铜等金属矿产资源和大量的二氧化硅、硫化物等,将为人类社会的可持续发展作出贡献.下列有关叙述正确的是( )
| A. | 月球上的二氧化硅所含元素都是第三周期元素 | |
| B. | 3He可发生核聚变反应,这是一种化学变化 | |
| C. | 月球上的3He是一种新元素 | |
| D. | 月球和地球上的钛、铁、铬、镍等原子应该具有相同的核外电子排布 |
2.下列事实不能用勒夏特列(平衡移动)原理解释的是( )


| A. | 开启啤酒瓶后,瓶中马上泛起大量泡沫 | |
| B. | 将收集NO2气体的烧瓶密闭后,放在装有热水的烧杯中,发生颜色变化 | |
| C. | 合成氨时采用铁触媒作反应催化剂 | |
| D. | 工业上生产硫酸的过程中使用过量的空气以提高二氧化硫的利用率 |
19.下列反应中,不属于四种基本反应类型的是( )
| A. | CuSO4+H2S═CuS↓+H2SO4 | B. | 2FeCl3+Cu═2FeCl2+CuCl2 | ||
| C. | Cu2(OH)2CO3$\frac{\underline{\;\;△\;\;}}{\;}$2CuO+CO2↑+H2O | D. | 4Fe(OH)2+O2+2H2O═4Fe(OH)3 |
6.下列说法正确的是( )
| A. | 检验淀粉溶液可以用碘化钾溶液 | |
| B. | 油脂在碱性条件下水解可以得到甘油和高级脂肪酸 | |
| C. | 向蛋白质溶液中加入饱和氯化铜溶液有固体析出,加入一定量水后固体不会溶解 | |
| D. | 乙烯使溴水褪色和使酸性高锰酸钾溶液褪色的原理是一样的 |
16.实验室用少量的溴水和足量的乙醇制备1,2-二溴乙烷的装置如下图所示:
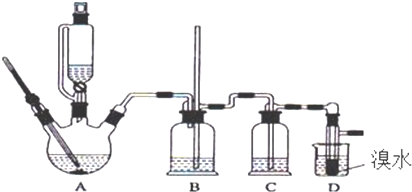
有关数据列表如下:
回答下列问题:
(1)烧瓶A中发生的主要的反应方程式CH3CH2OH$→_{170℃}^{浓硫酸}$CH2=CH2↑+H2O.
(2)装置B的作用是平衡压强,作安全瓶,防止倒吸.
(3)在装置C中应加入d (填字母).
a.水 b.浓硫酸 c.饱和碳酸氢钠溶液 d.氢氧化钠溶液
(4)若产物中有少量未反应的Br2,最好用e(填字母)洗涤除去.
a.水 b.氢氧化钠溶液 c.碘化钠溶液 d.乙醇 e.Na2SO3溶液
(5)若产物中有少量副产物乙醚,可用蒸馏的方法除去.
(6)反应过程中应用冷水冷却装置D,但又不能过度冷却(如用冰水),其原因是产品熔点低,过度冷却会凝固而堵塞导管口.
(7)判断该制备反应已经结束的最简单方法是D中溴水完全褪色.

有关数据列表如下:
| 乙醇 | 1,2-二溴乙烷 | 醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g•cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -l30 | 9 | -1l6 |
(1)烧瓶A中发生的主要的反应方程式CH3CH2OH$→_{170℃}^{浓硫酸}$CH2=CH2↑+H2O.
(2)装置B的作用是平衡压强,作安全瓶,防止倒吸.
(3)在装置C中应加入d (填字母).
a.水 b.浓硫酸 c.饱和碳酸氢钠溶液 d.氢氧化钠溶液
(4)若产物中有少量未反应的Br2,最好用e(填字母)洗涤除去.
a.水 b.氢氧化钠溶液 c.碘化钠溶液 d.乙醇 e.Na2SO3溶液
(5)若产物中有少量副产物乙醚,可用蒸馏的方法除去.
(6)反应过程中应用冷水冷却装置D,但又不能过度冷却(如用冰水),其原因是产品熔点低,过度冷却会凝固而堵塞导管口.
(7)判断该制备反应已经结束的最简单方法是D中溴水完全褪色.
20.氧化还原反应的实质是( )
| A. | 是否有电子转移 | |
| B. | 同一元素的化合价在反应前后是否有变化 | |
| C. | 是否有氧元素参加 | |
| D. | 是否是化合反应或分解反应 |
1.下列说法中不正确的是( )
| A. | 将化学能转变为电能的装置叫做原电池 | |
| B. | 乙醇和沼气都是可再生能源 | |
| C. | CO2是造成酸雨的主要原因之一 | |
| D. | 质子数相同而中子数不同的同一元素的不同原子互称为同位素 |
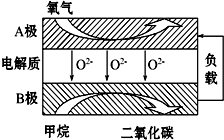 以甲烷为燃料的新型电池,其成本大大低于以氢气为燃料的传统燃料电池,目前得到广泛的研究,右图是目前研究较多的一类固体氧化物燃料电池的工作原理示意图.回答下列问题:
以甲烷为燃料的新型电池,其成本大大低于以氢气为燃料的传统燃料电池,目前得到广泛的研究,右图是目前研究较多的一类固体氧化物燃料电池的工作原理示意图.回答下列问题: