题目内容
下列表示对应化学反应的离子方程式正确的是( )
| A、将过量SO2通入少量氨水中:SO2+2NH3?H2O═2NH4++SO32- |
| B、实验室用Cu和稀HNO3反应制取少量NO气体:Cu+4H++NO3-═Cu2++NO↑+2H2O |
| C、NaHSO4溶液与Ba(OH)2溶液反应至中性:2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O |
| D、KIO3与KI在酸性溶液中反应:5I-+IO3-+3H2O═3I2+6OH- |
考点:离子方程式的书写
专题:离子反应专题
分析:A、过量SO2通入少量氨水,生成亚硫酸氢盐;
B、得失电子不守恒,导致电荷不守恒;
C、溶液反应至中性,说明氢离子和氢氧根离子的物质的量相等,所以硫酸根离子过量;
D、酸性溶液中不存在氢氧根离子.
B、得失电子不守恒,导致电荷不守恒;
C、溶液反应至中性,说明氢离子和氢氧根离子的物质的量相等,所以硫酸根离子过量;
D、酸性溶液中不存在氢氧根离子.
解答:
解:A、过量SO2通入少量氨水,生成亚硫酸氢盐,所以正确的离子反应方程式为:SO2+NH3?H2O═NH4++HSO3-,故A错误;
B、得失电子不守恒,导致电荷不守恒,所以正确的离子反应方程式为3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O,故B错误;
C、溶液反应至中性,说明氢离子和氢氧根离子的物质的量相等,所以硫酸根离子过量,正确的离子反应方程式为:2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O,故C正确;
D、酸性溶液中不存在氢氧根离子,正确的离子方程式为:5I-+IO3-+6H+═3I2+3H2O,故D错误;
故选C.
B、得失电子不守恒,导致电荷不守恒,所以正确的离子反应方程式为3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O,故B错误;
C、溶液反应至中性,说明氢离子和氢氧根离子的物质的量相等,所以硫酸根离子过量,正确的离子反应方程式为:2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O,故C正确;
D、酸性溶液中不存在氢氧根离子,正确的离子方程式为:5I-+IO3-+6H+═3I2+3H2O,故D错误;
故选C.
点评:本题考查离子方程式的书写,题目难度不大,注意从化学式、离子符号、电荷守恒以及是否符合反应实际的角度分析.

练习册系列答案
相关题目
NH3.H2O.CH4三分子中键角大小顺序正确的是( )
| A、NH3>H2O>CH4 |
| B、CH4>NH3>H2O |
| C、CH4>H2O>NH3 |
| D、H2O>CH4>NH3 |
下列有关物质的性质和该性质的应用均正确的是( )
| A、乙醇能够使蛋白质变性,可用于皮肤消毒 |
| B、Na的金属性比Mg强,可用Na与MgCl2溶液反应制取金属Mg |
| C、光照时乙烷和氯气能发生取代反应,工业上可用该反应生产氯乙烷 |
| D、碳酸钠溶液显碱性,用热的饱和碳酸钠溶液可除去金属表面的油污 |
关于金属腐蚀的以下叙述中错误的是( )
| A、铁器生锈、铜器长出“铜绿”、银制器皿表面变暗,都属于金属腐蚀 |
| B、生铁比软铁芯(几乎是纯铁)容易生锈 |
| C、铆在铜板上的铁钉在潮湿空气中容易生锈 |
| D、家用炒菜铁锅用水清洗放置后出现的锈斑主要成分是Fe3O4 |
同温同压下,某集气瓶充满CO2时为122g,充满O2时为116g,充满气体A时为114g,则A 的式量为( )
| A、60 | B、32 | C、44 | D、28 |
下列有关化学用语正确的是( )
A、Cl-离子的结构示意图: |
| B、乙醇的分子式:CH3CH2OH |
C、丙烷分子的比例模型示意图: |
D、甲烷的结构式为: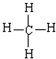 |
下列各组物质中,互为同位素的是( )
| A、H2O与H2O2 |
| B、CO2与CO |
| C、金刚石与石墨 |
| D、35Cl 与37Cl |
用价电子对互斥理论(VSEPR)可以预测许多分子或离子的空间构型,也可推测键角大小,下列判断正确的是( )
| A、CS2是V形分子 |
| B、SnBr2键角大于120° |
| C、BF3是三角锥形分子 |
| D、NH4+键角等于109.5° |
下列化学反应既是放热反应,同时又是氧化还原反应的是( )
| A、二氧化碳气体与碳单质高温下的反应 |
| B、八水合氢氧化钡固体与氯化铵固体的反应 |
| C、酸碱中和反应 |
| D、过氧化钠固体与二氧化碳气体的反应 |