题目内容
下列有关化学用语正确的是( )
A、Cl-离子的结构示意图: |
| B、乙醇的分子式:CH3CH2OH |
C、丙烷分子的比例模型示意图: |
D、甲烷的结构式为: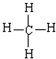 |
考点:原子结构示意图,分子式,球棍模型与比例模型
专题:化学用语专题
分析:A.氯离子核内质子数为17,有3个电子层,最外层有8个电子;
B.乙醇的分子式:C2H6O;
C.用小球和短棍表示有机物分子组成的模型为球棍模型;
D.甲烷分子的结构式 .
.
B.乙醇的分子式:C2H6O;
C.用小球和短棍表示有机物分子组成的模型为球棍模型;
D.甲烷分子的结构式
 .
.解答:
解:A.氯离子核内质子数为17,有3个电子层,最外层有8个电子,故氯离子的结构示意图为: ,故A错误;
,故A错误;
B.乙醇的分子式:C2H6O,结构简式为:C2H5OH或CH3CH2OH,故B错误;
C.丙烷结构简式为CH3CH2CH3,其丙烷分子的球棍模型为: ,故C错误;
,故C错误;
D.甲烷的结构式为: ,故D正确;
,故D正确;
故选D.
 ,故A错误;
,故A错误;B.乙醇的分子式:C2H6O,结构简式为:C2H5OH或CH3CH2OH,故B错误;
C.丙烷结构简式为CH3CH2CH3,其丙烷分子的球棍模型为:
 ,故C错误;
,故C错误;D.甲烷的结构式为:
 ,故D正确;
,故D正确;故选D.
点评:本题考查了结构式、分子式、原子结构示意图、球棍模型表示方法判断,题目难度中等,注意掌握常见的化学用语的概念及正确表示方法.

练习册系列答案
相关题目
根据表中信息,判断下列叙述中正确的是( )
| 序号 | 氧化剂 | 还原剂 | 其他反应物 | 氧化产物 | 还原产物 |
| ① | Cl2 | FeBr2 | Cl- | ||
| ② | KMnO4 | H2O2 | H2SO4 | O2 | Mn2+ |
| ③ | KClO3 | 浓盐酸 | Cl2 |
| A、表中①组反应可能有一种或两种元素被氧化 |
| B、表中②组反应的离子方程式是2MnO4-+3H2O2+6H+═2Mn2++4O2↑+6H2O |
| C、表中③组反应的还原产物是KCl,电子转移数目是6e- |
| D、氧化性强弱比较:KClO3>Fe3+>Cl2>Br2 |
下表是某同学血常规检查报告单的部分内容,这位同学应该注意补充的微量元素是( )
| 项目 | 结果 | 正常范围参考值 | 单位 | |
| 1 | 红细胞计数 | 2.3 | 3.5~5 | 1×1012/L |
| 2 | 血红蛋白 | 75 | 110~150 | g/L |
| 3 | 血小板计数 | 205.5 | 100~300 | 109/L |
| A、碘 | B、硒 | C、铁 | D、锌 |
下列说法不正确的是( )
| A、石英光导纤维,在遇到强碱或氢氟酸时均可能发生“断路” |
| B、葡萄糖既能发生银镜反应,又能发生水解反应 |
| C、浓硝酸和醋酸铅溶液均可使鸡蛋清溶液中的蛋白质变性 |
| D、1mol油脂完全水解的产物是1mol甘油和3mol高级脂肪酸(或盐) |
下列表示对应化学反应的离子方程式正确的是( )
| A、将过量SO2通入少量氨水中:SO2+2NH3?H2O═2NH4++SO32- |
| B、实验室用Cu和稀HNO3反应制取少量NO气体:Cu+4H++NO3-═Cu2++NO↑+2H2O |
| C、NaHSO4溶液与Ba(OH)2溶液反应至中性:2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O |
| D、KIO3与KI在酸性溶液中反应:5I-+IO3-+3H2O═3I2+6OH- |
大量存在于葡萄中,在加热条件下,能和银氨溶液反应生成银镜的物质是( )
| A、葡萄糖 | B、淀粉 |
| C、纤维素 | D、乙酸 |
在氧化还原反应CuO+H
Cu+H2O中,氧化剂是( )
| ||
| A、CuO |
| B、H2 |
| C、Cu |
| D、H2O |
酸式盐是盐的一种,可看作是多元酸中的氢离子未被完全中和所得到的盐,常见的有NaHCO3、NaHSO4、KH2PO4、K2HPO4等.已知H3PO2(次磷酸)与足量的NaOH反应只生成一种盐NaH2PO2,则下列说法正确的是( )
| A、H3PO2属于二元酸 |
| B、H3PO2属于三元酸 |
| C、NaH2PO2属于酸式盐 |
| D、NaH2PO2属于正盐 |
足量锌片和100mL5mol/L的稀H2SO4反应时,为减慢反应速率,又不影响生成氢气的总量,可采用的方法是( )
| A、加入几滴CuSO4溶液 |
| B、加入少量水 |
| C、升高温度 |
| D、加入少量Na2CO3 |