题目内容
在一密闭容器中充入1molH2和1molI2,压强为P(Pa),并在一定温度下使其发生反应达到平衡状态:
H2(g)+I2(g)?2HI(g)△H<0 H<0
(1)保持容器体积不变,向其中再加入1molH2,反应速率(填“加快”、“减慢”、“不变”或“无法确定”下同) ,平衡(填“向左”、“向右”、“不”或“无法判断”,下同) 移动.
(2)保持容器体积不变,向其中加入1molN2,反应速率 ,平衡 移动.
(3)保持容器内压强不变,向其中加入1molN2,反应速率 ,平衡 移动.
(4)保持容器内压强不变,向其中再加入1molH2(g)和1molI2(g),反应速率 ,平衡 移动.
H2(g)+I2(g)?2HI(g)△H<0 H<0
(1)保持容器体积不变,向其中再加入1molH2,反应速率(填“加快”、“减慢”、“不变”或“无法确定”下同)
(2)保持容器体积不变,向其中加入1molN2,反应速率
(3)保持容器内压强不变,向其中加入1molN2,反应速率
(4)保持容器内压强不变,向其中再加入1molH2(g)和1molI2(g),反应速率
考点:化学平衡的影响因素
专题:
分析:在恒定温度下,反应速率的影响因素取决于浓度和压强,浓度越大,反应速率越大,如通入惰性气体,参加反应的物质的浓度不变,则反应速率不变,如压强不变,通入惰性气体,但体积增大,反应物的浓度减小,则反应速率减小,温度越高反应速率越快,使用正催化剂加快化学反应速率,以此解答该题.
解答:
解:(1)保持容器容积不变,向其中加入1molH2,增大反应物浓度,反应速率增大,平衡右移,故答案为:加快;向右;
(2)保持容器体积不变,向其中加入1mol N2,反应物的浓度不变,则反应速率不变,平衡不移动,故答案为:不变;
(3)保持容器内气体压强不变,向其中加入1mol N2,体积增大,反应物的浓度减小,则反应速率减小,由于反应是气体体积不变的反应,平衡不移动,
故答案为:降低;不;
(4)保持容器内气体压强不变,向其中加入1 mol H2(g)和1molI2(g),因体积增大为2倍,物质的量增大为2倍,则浓度不变,反应速率不变,平衡也移动.
故答案为:不变;不.
(2)保持容器体积不变,向其中加入1mol N2,反应物的浓度不变,则反应速率不变,平衡不移动,故答案为:不变;
(3)保持容器内气体压强不变,向其中加入1mol N2,体积增大,反应物的浓度减小,则反应速率减小,由于反应是气体体积不变的反应,平衡不移动,
故答案为:降低;不;
(4)保持容器内气体压强不变,向其中加入1 mol H2(g)和1molI2(g),因体积增大为2倍,物质的量增大为2倍,则浓度不变,反应速率不变,平衡也移动.
故答案为:不变;不.
点评:本题考查了化学反应速率、化学平衡影响因素分析判断,平衡移动原理应用,平衡常数计算分析,掌握基础是关键,题目较简单.

练习册系列答案
相关题目
在1100℃,一定容积的密闭容器中发生反应:FeO(s)+CO(g)?Fe(s)+CO2(g)△H=a kJ/mol(a>0),该温度下K=0.263,下列有关该反应的说法正确的是( )
| A、若生成1molFe,则放出a kJ热量 |
| B、若升高温度,则正反应速率加快,逆反应速率减慢,化学平衡正向移动 |
| C、若容器内压强不随时间变化,则可以判断该反应已达到化学平衡状态 |
| D、达到化学平衡状态时,若c(CO)=0.100 kJ/mol,则c(CO2)=0.0263 kJ/mol |
 在密闭容器中进行下列反应:(g)+N(g)?R(g)+2L,在不同条件下R的百分含量R%的变化情况如下图,下列叙述正确的是( )
在密闭容器中进行下列反应:(g)+N(g)?R(g)+2L,在不同条件下R的百分含量R%的变化情况如下图,下列叙述正确的是( )| A、正反应吸热,L是气体 |
| B、正反应吸热,L是固体 |
| C、正反应放热,L是气体 |
| D、正反应放热,L是固体或液体 |
在一固定容积的密闭容器中:mA(g)+nB(g)?pC(g)+qD(s),当m、n、p、q为任意整数(不为零)时,能说明体系达到平衡状态的标志是①p v (A)正=m v (C)逆;②体系的压强不再改变;③混合气体的密度不再改变;④反应速率vA:vB:vC:vD=m:n:p:q;⑤当m+n=p时,混合气体的平均相对分子质量不再改变;( )
| A、①③⑤ | B、①②⑤ |
| C、②③④ | D、①②④ |
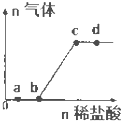 向Na2CO3、NaHCO3混合溶液中逐滴加入稀盐酸,生成气体的量随盐酸加入量的变化关系如右图所示.则下列离子组在对应的溶液中一定能大量共存的是( )
向Na2CO3、NaHCO3混合溶液中逐滴加入稀盐酸,生成气体的量随盐酸加入量的变化关系如右图所示.则下列离子组在对应的溶液中一定能大量共存的是( )| A、a点对应的溶液中:Na+、OH-、SO42-、NO3- |
| B、b点对应的溶液中:Al3+、Fe3+、NO3-、Cl- |
| C、c点对应的溶液中:Na+、Ca2+、NO3-、Cl- |
| D、d点对应的溶液中:Cl-、NO3-、Fe2+、Na+ |
一定温度下,反应A2(g)+B2(g)?2AB(g)达到平衡.下列说法中,正确的是( )
| A、A、B、AB的物质的量浓度之比一定为1:1:2 |
| B、A、B全部转化为AB |
| C、容器内各物质的浓度不随时间变化 |
| D、单位时间内减少x mol A2,同时生成2x mol AB |
pH相同的醋酸溶液和盐酸,分别用蒸馏水稀释到原溶液的m倍和n倍,稀释后两溶液的pH仍相同,则m和n的关系量是( )
| A、m=n | B、m>n |
| C、m<n | D、无法判断 |
已知2KClO3+I2═2KIO3+Cl2↑,下列对此反应的说法正确的是( )
| A、氧化产物与还原产物的物质的量之比为1:2 |
| B、I2的还原性强于Cl2 |
| C、标准状况下产生11.2 L Cl2,转移电子为1 mol |
| D、Cl2和I2都是氧化剂 |