题目内容
用化学术语回答下列问题:
(1)书写电离方程式①氢氧化铁 ②氢溴酸
(2)书写水解离子方程式①次氯酸钠溶液 ②硫酸铝与硫化钠混合溶液
(3)电解硝酸银溶液电极反应式(惰性电极)
①阳极:
②阴极: .
(1)书写电离方程式①氢氧化铁
(2)书写水解离子方程式①次氯酸钠溶液
(3)电解硝酸银溶液电极反应式(惰性电极)
①阳极:
②阴极:
考点:电离方程式的书写,离子方程式的书写,电极反应和电池反应方程式
专题:
分析:(1)书写电离方程式首先应判断电解质的强弱确定使用等号还是可逆号,强电解质完全电离,弱电解质部分电离,多元弱酸分步电离,多元弱碱一步写到位;
(3)书写水解反应的离子方程式先确定水解离子,依据水解规律写出水解的离子方程式,注意电荷守恒;
(3)电解池书写电极反应式,应先确定电极名称,然后找出放电离子,依据氧化还原反应规律书写,注意电荷、得失电子数应守恒.
(3)书写水解反应的离子方程式先确定水解离子,依据水解规律写出水解的离子方程式,注意电荷守恒;
(3)电解池书写电极反应式,应先确定电极名称,然后找出放电离子,依据氧化还原反应规律书写,注意电荷、得失电子数应守恒.
解答:
解:(1)①氢氧化铁为弱电解质,部分电离,电离方程式为:Fe(OH)3?3OH-+Fe3+;
故答案为:Fe(OH)3 ?3OH-+Fe3+;
②氢溴酸为强电解质,完全电离,电离方程式为:HBr=H++Br-;
故答案为:HBr=H++Br-;
(2)①次氯酸钠为强碱弱酸盐,水解生成次氯酸和氢氧化钠,离子方程式为:ClO-+H2O?HClO+OH-;
故答案为:ClO-+H2O?HClO+OH-;
②硫酸铝与硫化钠混合溶液,铝离子与硫离子发生双水解,离子方程式为:Al3++3S2-+6H2O=2Al(OH)3↓+3H2S↑;
故答案为:Al3++3S2-+6H2O=2Al(OH)3↓+3H2S↑;
(3)用惰性电极电解硝酸银溶液,阳极氢氧根离子放电,电极反应式为:4OH--4e-=2H2O+O2↑;
故答案为:4OH--4e-=2H2O+O2↑;
阴极银离子放电,电极反应式为:Ag++e-=Ag;
故答案为:Ag++e-=Ag.
故答案为:Fe(OH)3 ?3OH-+Fe3+;
②氢溴酸为强电解质,完全电离,电离方程式为:HBr=H++Br-;
故答案为:HBr=H++Br-;
(2)①次氯酸钠为强碱弱酸盐,水解生成次氯酸和氢氧化钠,离子方程式为:ClO-+H2O?HClO+OH-;
故答案为:ClO-+H2O?HClO+OH-;
②硫酸铝与硫化钠混合溶液,铝离子与硫离子发生双水解,离子方程式为:Al3++3S2-+6H2O=2Al(OH)3↓+3H2S↑;
故答案为:Al3++3S2-+6H2O=2Al(OH)3↓+3H2S↑;
(3)用惰性电极电解硝酸银溶液,阳极氢氧根离子放电,电极反应式为:4OH--4e-=2H2O+O2↑;
故答案为:4OH--4e-=2H2O+O2↑;
阴极银离子放电,电极反应式为:Ag++e-=Ag;
故答案为:Ag++e-=Ag.
点评:本题考查了电离方程式、水解反应离子方程式、电极反应式书写,是高考频考点,明确各种式子书写方法和注意问题是解题关键,题目难度不大.

练习册系列答案
 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案
相关题目
下列物质中,不属于电解质的是( )
| A、Cu |
| B、NaCl |
| C、NH3 |
| D、H2SO4 |
利用下列各组物质制备和收集相应的气体,可采用如图所示装置(图中尾气处理装置略)的是( )①石灰石和稀盐酸;②二氧化锰和浓盐酸;③铜和稀硝酸;④铜和浓硫酸;⑤双氧水和二氧化锰;⑥铝和烧碱溶液.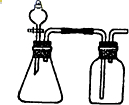

| A、①③ | B、①⑤ | C、④⑤ | D、⑤⑥ |
工业上用氮气和氢气合成氨:N2+3H2
2NH3(反应放热),从反应速率和化学平衡两方面看,合成氨的适宜条件一般为压强:20MPa-50MPa,温度:500℃左右,催化剂:铁触媒.下列有关合成氨工业的叙述不正确的是( )
| 催化剂 |
| 高温高压 |
| A、使用铁触媒,可使氮气和氢气混合气体之间的反应在较低温度下取得较高的反应速率 |
| B、工业上选择上述条件下合成氨,可以使氮气全部转化为氨 |
| C、上述化学平衡的移动受到温度、反应物的浓度、压强等因素的影响 |
| D、温度升高,不利于氮气的转化率 |
如表所示,提纯下列物质(括号内为杂质),所用除杂试剂和分离方法都正确的是( )
| 序号 | 不纯物 | 除杂试剂 | 分离方法 |
| A | CH4(C2H4) | 酸性KMnO4溶液 | 洗气 |
| B | 苯(苯酚) | 溴水 | 过滤 |
| C | 乙酸乙酯(乙酸) | NaOH溶液 | 蒸馏 |
| D | KNO3(NaCl) | 水 | 重结晶 |
| A、A | B、B | C、C | D、D |
下列物质反应过程中不会产生气体的是( )
A、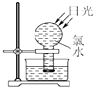 |
B、 |
C、 |
D、 |