题目内容
已知2KClO3+I2═2KIO3+Cl2↑,下列对此反应的说法正确的是( )
| A、氧化产物与还原产物的物质的量之比为1:2 |
| B、I2的还原性强于Cl2 |
| C、标准状况下产生11.2 L Cl2,转移电子为1 mol |
| D、Cl2和I2都是氧化剂 |
考点:氧化还原反应
专题:氧化还原反应专题
分析:从元素化合价的角度判断氧化产物、还原产物,氧化还原反应中氧化还原反应中氧化剂和还原剂之间得失电子数目相等,根据化合价的变化可计算转移电子的物质的量,反应中还原剂的还原性大于还原产物的还原性,以此解答该题.
解答:
解:A.在反应2KClO3+I2=2KIO3+Cl2中,氧化产物为KIO3,还原产物为I2,由化学计量数可知,氧化产物与还原产物的物质的量比为1:2,故A错误;
B.在反应2KClO3+I2=2KIO3+Cl2中,还原剂为I2,还原产物为Cl2,还原剂的还原性大于还原产物的还原性,则I2的还原性强于Cl2,故B正确;
C.n(Cl2)=
=0.5mol,Cl元素化合价由+5价→0价,则转移的电子的物质的量为0.5mol×5×2=5mol,故C错误;
D.该反应中KClO3中Cl的化合价降低被还原作氧化剂,I2的化合价升高作还原剂,故D错误.
故选B.
B.在反应2KClO3+I2=2KIO3+Cl2中,还原剂为I2,还原产物为Cl2,还原剂的还原性大于还原产物的还原性,则I2的还原性强于Cl2,故B正确;
C.n(Cl2)=
| 11.2L |
| 22.4L/mol |
D.该反应中KClO3中Cl的化合价降低被还原作氧化剂,I2的化合价升高作还原剂,故D错误.
故选B.
点评:本题考查氧化还原反应的知识,题目难度不大,注意通过化学方程式结合化合价的变化判断氧化剂、还原剂以及氧化产物、还原产物之间的物质的量的关系.

练习册系列答案
 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案
相关题目
为检验FeCl2是否变质,可向溶液试样中加入( )
| A、NaOH溶液 | B、KSCN |
| C、铁粉 | D、石蕊试液 |
下列操作过程中使溶液导电性基本不变的是( )
| A、100ml自来水中加入0.01molNaOH固体 |
| B、100ml 0.5mol/L的NaOH中通入0.05mol氯气 |
| C、100ml0.5mol/L的醋酸中加入100ml 0.5mol/L的氨水 |
| D、100ml 0.1mol/L的氯水中通入0.01molSO2气体 |
对下列物质:①H2SO4、②CO2、③液态NaOH、④BaSO4、⑤NH3、⑥SO2、⑦NH3?H2O、⑧C2H5OH、⑨Cu、⑩氯化钠溶液按要求分类正确的是( )
| A、能导电的:③、⑦、⑨、⑩ |
| B、电解质:①、③、④、⑦、⑩ |
| C、非电解质:②、⑤、⑥、⑧、⑨ |
| D、强电解质:①、③、④ |
下列各图所反映的措施中,目的是为了加快其化学反应速率的是( )
A、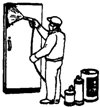 铁门表面喷漆 |
B、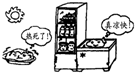 冰箱保存食物 |
C、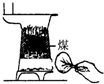 扇子扇煤炉火 |
D、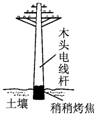 |
浙江海洋经济发展示范区建设已上升为国家战略,海洋经济将成为浙江经济转型升级发展的重点.下列说法不正确的是( )
| A、从海水中提取溴单质的过程中涉及氧化还原反应 |
| B、从海带中提取碘单质的过程中涉及置换反应 |
| C、从海水中提取氯化钠的过程中涉及化学反应 |
| D、电解饱和食盐水制氯气的过程中涉及氧化还原反应 |
同温同压下,等质量的SO2和CO2相比较,下列叙述中正确的是( )
| A、电子数之比1:1 |
| B、体积比16:11 |
| C、密度比16:11 |
| D、氧原子数之比为1:1 |