题目内容
下列表示对应化学反应的离子方程式正确的是( )
| A、用氯化铁溶液腐蚀铜板:Cu+Fe3+═Cu2++Fe2+ | ||
| B、用KIO3氧化酸性溶液中的KI:5I-+IO3-+3H2O═3I2+6OH- | ||
C、2-溴丙酸在氢氧化钠热溶液中水解:CH3CHBrCOOH+2OH-
| ||
| D、硝酸铁稀溶液中加入足量稀氢碘酸:6I-+2NO3-+8H+═3I2+2NO↑+4H2O |
考点:离子方程式的书写
专题:离子反应专题
分析:A.根据电荷守恒判断,该离子方程式两边电荷不守恒;
B.在酸性溶液中的反应,反应产物不可能为氢氧根离子;
C.卤代烃在氢氧化钠的水溶液中水解生成醇羟基、羧基与氢氧化钠发生中和反应;
D.氢碘酸足量,铁离子能够将碘离子氧化成碘单质.
B.在酸性溶液中的反应,反应产物不可能为氢氧根离子;
C.卤代烃在氢氧化钠的水溶液中水解生成醇羟基、羧基与氢氧化钠发生中和反应;
D.氢碘酸足量,铁离子能够将碘离子氧化成碘单质.
解答:
解:A.用氯化铁溶液腐蚀铜板,铁与铜离子反应生成铜离子和亚铁离子,正确的离子方程式为:Cu+2Fe3+═Cu2++2Fe2+,故A错误;
B.KIO3氧化酸性溶液中的KI,反应产物不可能为氢氧根离子,正确的离子方程式为:5I-+IO3-+6H+═3I2+3H2O,故B错误;
C.2-溴丙酸在氢氧化钠热溶液中水解,反应的离子方程式为:CH3CHBrCOOH+2OH-
CH3CH(OH)COO-+Br-+H2O,故C正确;
D.硝酸铁稀溶液中加入足量稀氢碘酸,铁离子能够将碘离子氧化成碘单质,正确的离子方程式为:10I-+3NO3-+Fe3++12H+═5I2+3NO↑+Fe2++6H2O,故D错误;
故选C.
B.KIO3氧化酸性溶液中的KI,反应产物不可能为氢氧根离子,正确的离子方程式为:5I-+IO3-+6H+═3I2+3H2O,故B错误;
C.2-溴丙酸在氢氧化钠热溶液中水解,反应的离子方程式为:CH3CHBrCOOH+2OH-
| △ |
D.硝酸铁稀溶液中加入足量稀氢碘酸,铁离子能够将碘离子氧化成碘单质,正确的离子方程式为:10I-+3NO3-+Fe3++12H+═5I2+3NO↑+Fe2++6H2O,故D错误;
故选C.
点评:本题考查了离子方程式的正误判断,该题是高考中的高频题,属于中等难度的试题,注意明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等)、检查是否符合原化学方程式等,选项D为易错点,注意碘离子能够被铁离子氧化.

练习册系列答案
相关题目
描述CH3-CH=CH-C≡C-CF3分子结构下列叙述中,正确的是( )
| A、6个碳原子有可能都在一条直线上 |
| B、6个碳原子不可能都在一条直线上 |
| C、6个碳原子不可能都在一个平面上 |
| D、所有原子可能都在一个平面上 |
下列顺序正确的是( )
| A、熔点:SiO2<NaF<KCl |
| B、水溶性:NH3<SO2<HCl |
| C、酸性:HF>HCl>HI |
| D、碱性:Mg(OH)2<KOH<RbOH |
下列四种元素中,非金属性最强的是( )
| A、Cl | B、P | C、S | D、Si |
下列说法正确的是( )
| A、常温下醋酸分子不可能存在于pH>7的碱性溶液中 |
| B、常温下向氯化铵溶液中加入少量氨水使溶液的pH=7,则混合溶液中c(Cl-)>c(NH4+) |
| C、0.1 mol?L-1的氯化铵溶液与0.05 mol?L-1的氢氧化钠溶液等体积混合,溶液中离子浓度c(Cl-)>c(NH4+)>c(Na+)>c(OH-) |
| D、0.1 mol?L-1硫化钠溶液中离子浓度关系c(OH-)=c(H+)+c(HS-)+c(H2S) |
下列表示式错误的是( )
A、氯化钠的电子式: |
| B、过氧化氢的结构式:H-O-O-H |
C、HCl的电子式: |
D、铝原子的结构示意图: |
研究反应物的化学计量数与产物之间的关系时,使用类似数轴的方法可以收到的直观形象的效果.下列表达不正确的是( )
A、CO2通入澄清的石灰水中反应的产物: |
B、Fe在Cl2中的燃烧产物: |
C、AlCl3溶液中滴加NaOH后铝的存在形式: |
D、氨水与SO2反应后溶液中的铵盐: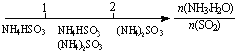 |
2013年10月世界卫生组织癌症专门机构首次指认大气污染“对人类致癌”,下列行为有利于防止大气污染、遏制雾霾天气发生的是( )
| A、在田间焚烧秸杆 |
| B、冬季燃烧大量烟煤供热取暖 |
| C、提倡开私家车出行,减少乘坐公交车 |
| D、改善能源结构,大力发展太阳能、风能等清洁能源 |
NA代表阿伏加德罗常数,下列叙述错误的是( )
| A、1mol任何物质所含有的原子数为NA |
| B、在H2O2+Cl2═2HCl+O2反应中,每生成32g氧气,则转移2NA个电子 |
| C、标准状况下,分子数为NA的CO、C2H4混合气体体积约为22.4L,质量为28g |
| D、17克氨气所含的电子数为10NA |