题目内容
研究反应物的化学计量数与产物之间的关系时,使用类似数轴的方法可以收到的直观形象的效果.下列表达不正确的是( )
A、CO2通入澄清的石灰水中反应的产物: |
B、Fe在Cl2中的燃烧产物: |
C、AlCl3溶液中滴加NaOH后铝的存在形式: |
D、氨水与SO2反应后溶液中的铵盐: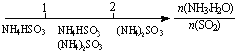 |
考点:氯、溴、碘及其化合物的综合应用,二氧化硫的化学性质,镁、铝的重要化合物
专题:图示题,计算题
分析:A.根据发生的反应Ca(OH)2+CO2═CaCO3↓+H2O;CaCO3+CO2+H2O═Ca(HCO3)2分析;
B.Fe在Cl2中燃烧的产物与Fe和Cl2的用量无关,其产物只有FeCl3;
C.根据可能发生的反应Al3++3OH-=Al(OH)3↓,Al3++4OH-=AlO2-+2H2O分析;
D.根据可能发生的反应有:NH3?H2O+SO2=NH4HSO3,2NH3?H2O+SO2=(NH4)2SO3+H2O进行分析.
B.Fe在Cl2中燃烧的产物与Fe和Cl2的用量无关,其产物只有FeCl3;
C.根据可能发生的反应Al3++3OH-=Al(OH)3↓,Al3++4OH-=AlO2-+2H2O分析;
D.根据可能发生的反应有:NH3?H2O+SO2=NH4HSO3,2NH3?H2O+SO2=(NH4)2SO3+H2O进行分析.
解答:
解:A.反应的化学方程式:Ca(OH)2+CO2═CaCO3↓+H2O;CaCO3+CO2+H2O═Ca(HCO3)2,CO2与Ca(OH)2的物质的量之比为1:1时,恰好反应生成CaCO3,即CO2与Ca(OH)2的物质的量之比为≤1时反应得到CaCO3,CO2与Ca(OH)2的物质的量之比为2:1时,恰好反应生成Ca(HCO3)2,即CO2与Ca(OH)2的物质的量之比为≥2时反应得到Ca(HCO3)2,故A错误;
B.Fe在Cl2中燃烧只有一种产物FeCl3,故B错误;
C.Al3++3OH-=Al(OH)3↓,Al3++4OH-=AlO2-+2H2O,
<3,铝元素以Al3+和Al(OH)3形式存在;
=3,则以Al(OH)3形式存在;3<
<4以 AlO2-和Al(OH)3形式存在;
≥4只以 AlO2-形式存在,故C正确;
D.NH3?H2O+SO2=NH4HSO3,2NH3?H2O+SO2=(NH4)2SO3+H2O,
≤1,生成NH4HSO3;1<
<2,产物为NH4HSO3与(NH4)2SO3混合物;
≥2,只生成(NH4)2SO3,故D正确.
故选AB.
B.Fe在Cl2中燃烧只有一种产物FeCl3,故B错误;
C.Al3++3OH-=Al(OH)3↓,Al3++4OH-=AlO2-+2H2O,
| n(NaOH) |
| n(AlCl3) |
| n(NaOH) |
| n(AlCl3) |
| n(NaOH) |
| n(AlCl3) |
| n(NaOH) |
| n(AlCl3) |
D.NH3?H2O+SO2=NH4HSO3,2NH3?H2O+SO2=(NH4)2SO3+H2O,
| n(NH3?H2O) |
| n(SO2) |
| n(NH3?H2O) |
| n(SO2) |
| n(NH3?H2O) |
| n(SO2) |
故选AB.
点评:此题是近年以来出现的一道很少出现的试题题型题,是一道新情景试题,具有很强的综合性,也具有极强的迷惑性,各选项具有很强的干扰性,是一道好题!很容易选错答案.主要考查学生对元素化合物知识的掌握情况.注意Fe在Cl2中燃烧的产物与Fe和Cl2的用量无关,其产物只有FeCl3.

练习册系列答案
相关题目
阿魏酸在食品、医药等方面有着广泛用途.一种合成阿魏酸的反应可表示为:

下列说法正确的是( )

下列说法正确的是( )
| A、可用KMnO4酸性溶液检测上述反应是否有阿魏酸生成 |
| B、香兰素、阿魏酸均可与NaHCO3、NaOH溶液反应 |
| C、通常条件下,香兰素、阿魏酸都能发生取代、加成、消去反应 |
| D、与香兰素互为同分异构体,分子中有4种不同化学环境的氢,且能发生银镜反应的酚类化合物共有2种 |
a mol FeS与b mol Fe3O4投入到V L c mol?L-1的硝酸溶液中恰好完全反应,假设只产生NO气体.所得澄清溶液的成分是Fe(NO3)3和H2SO4的混合液,则反应中未被还原的硝酸为( )
| A、(a+3b) mol | ||
B、
| ||
C、
| ||
| D、(cV-3a-9b) mol |
下列表示对应化学反应的离子方程式正确的是( )
| A、用氯化铁溶液腐蚀铜板:Cu+Fe3+═Cu2++Fe2+ | ||
| B、用KIO3氧化酸性溶液中的KI:5I-+IO3-+3H2O═3I2+6OH- | ||
C、2-溴丙酸在氢氧化钠热溶液中水解:CH3CHBrCOOH+2OH-
| ||
| D、硝酸铁稀溶液中加入足量稀氢碘酸:6I-+2NO3-+8H+═3I2+2NO↑+4H2O |
 某学生设计了一个“黑笔写红字”的趣味实验.滤纸先用氯化钠、无色酚酞的混合液浸湿,然后平铺在一块铂片上,接通电源后,用铅笔在滤纸上写字,会出现红色字迹.据此下列叙述正确的是( )
某学生设计了一个“黑笔写红字”的趣味实验.滤纸先用氯化钠、无色酚酞的混合液浸湿,然后平铺在一块铂片上,接通电源后,用铅笔在滤纸上写字,会出现红色字迹.据此下列叙述正确的是( )| A、铅笔芯作阳极,发生氧化反应 |
| B、a为电源的正极 |
| C、铅笔尖附近有少量的氯气产生 |
| D、红字是H+放电,c(OH-)增大造成 |
 X、Y、Z、W均为中学化学的常见物质,一定条件下它们之间有如图转化关系(其它产物已略去),下列说法不正确的是( )
X、Y、Z、W均为中学化学的常见物质,一定条件下它们之间有如图转化关系(其它产物已略去),下列说法不正确的是( )| A、若W是单质铁,则Z溶液可能是FeCl2溶液 |
| B、若W是氢氧化钠,则X与Z可反应生成Y |
| C、若X是金属铝,则W可能是NaOH溶液 |
| D、若X为甲醇,则X、Z的相对分子质量可能相差14 |
下列不能说明氯元素的非金属性比硫元素强的事实是( )
①HCl比H2S稳定 ②HClO氧化性比H2SO4强 ③HClO4酸性比H2SO4强 ④氯原子最外层有7个电子,硫原子最外层有6个电子.
①HCl比H2S稳定 ②HClO氧化性比H2SO4强 ③HClO4酸性比H2SO4强 ④氯原子最外层有7个电子,硫原子最外层有6个电子.
| A、①②④ | B、①③ | C、②④ | D、③④ |
某有机物分子式为C8H10O,实验证明该有机物能与钠反应放出氢气,红外光谱显示苯环上有两个取代基团,则其可能的结构有几种( )
| A、5种 | B、6种 | C、7种 | D、8种 |
下列递变规律正确的是( )
| A、HClO4、H2SO4、H3PO4的酸性依次减弱 |
| B、HCl、HBr、HI的稳定性依次增强 |
| C、钠、镁、铝的还原性依次减弱 |
| D、P、S、Cl最高正价依次降低 |