题目内容
20.某反应过程能量变化如图所示,下列说法正确的是( )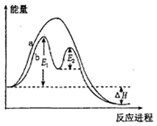
| A. | 反应过程a有催化剂参与 | |
| B. | 该反应为吸热反应 | |
| C. | 改变催化剂,可改变该反应的活化能 | |
| D. | 有催化剂条件下,反应的活化能等于E1+E2 |
分析 从图上分析,反应物能量高于生成物,正反应是放热反应,b过程活化能较低,可为加入催化剂,以此解答该题.
解答 解:A.b过程活化能较低,加入催化剂,故A错误;
B.反应物能量高于生成物,正反应是放热反应,故B错误;
C.不同的催化剂的催化效果不同,则改变的活化能不同,故C正确;
D.E1是反应物的活化能,E2是中间产物的活化能,故D错误.
故选C.
点评 本题考查化学反应与能量的变化,为高频考点,侧重于学生的分析能力的考查,注意相关基础知识的积累,难度不大.

练习册系列答案
 一线名师权威作业本系列答案
一线名师权威作业本系列答案
相关题目
10.c(H+)相同的盐酸溶液和醋酸溶液分别与锌反应,若最后锌都己完全溶解,但放出的气体一样多,则下列判断正确的是( )
| A. | 整个反应阶段平均速率:醋酸>盐酸 | B. | 反应所需时间:醋酸>盐酸 | ||
| C. | 参加反应的锌质量:盐酸>醋酸 | D. | 开始,反应速率:盐酸>醋酸 |
5.化学方程式为3MnO2+6KOH+KClO3$\frac{\underline{\;\;△\;\;}}{\;}$3K2MnO4+KCl+3H2O,下列说法中正确的( )
| A. | 反应中MnO2是氧化剂 | |
| B. | 该反应属于复分解反应 | |
| C. | KClO3在反应中失去电子 | |
| D. | 反应中每生成l mol K2MnO4,氧化剂得到2 mol电子 |
20.如表是元素周期表的一部分,针对所给的10种元素,完成下列各小题.
(1)第3周期中金属性最强的元素是钠(填“钠”或“镁”);
(2)S原子结构示意图为 ;钙离子的电子式为:Ca2+.
;钙离子的电子式为:Ca2+.
(3)第3周期元素中,最高价氧化物对应水化物酸性最强的是HClO4(填“H2SO4”或“HClO4”);
(4)C、N和O原子半径由小到大的顺序的是O<N<C;
(5)第3周期中气态氢化物最稳定的是HCl;(填“H2S”或“HCl”)
(6)Si是带来人类文明的重要元素之一,其氧化物化学式是SiO2;
(7)N元素形成的一种氢化物其水溶液呈碱性,请写出氢化物的化学式是NH3.
(8)铝是大自然赐予人类的宝物.它其中的一个用途是作为铝热剂,请写出铝和三氧化二铁发生反应的方程式2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3.
| 主族 周期 | I A | II A | III A | IV A | V A | VI A | VII A | 0 |
| 2 | C | N | O | |||||
| 3 | Na | Mg | Si | S | Cl | Ar | ||
| 4 | Ca |
(2)S原子结构示意图为
 ;钙离子的电子式为:Ca2+.
;钙离子的电子式为:Ca2+.(3)第3周期元素中,最高价氧化物对应水化物酸性最强的是HClO4(填“H2SO4”或“HClO4”);
(4)C、N和O原子半径由小到大的顺序的是O<N<C;
(5)第3周期中气态氢化物最稳定的是HCl;(填“H2S”或“HCl”)
(6)Si是带来人类文明的重要元素之一,其氧化物化学式是SiO2;
(7)N元素形成的一种氢化物其水溶液呈碱性,请写出氢化物的化学式是NH3.
(8)铝是大自然赐予人类的宝物.它其中的一个用途是作为铝热剂,请写出铝和三氧化二铁发生反应的方程式2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3.
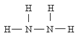 )可作为火箭发动机的燃料,NH3与NaClO反应可得到肼.
)可作为火箭发动机的燃料,NH3与NaClO反应可得到肼.