题目内容
10.c(H+)相同的盐酸溶液和醋酸溶液分别与锌反应,若最后锌都己完全溶解,但放出的气体一样多,则下列判断正确的是( )| A. | 整个反应阶段平均速率:醋酸>盐酸 | B. | 反应所需时间:醋酸>盐酸 | ||
| C. | 参加反应的锌质量:盐酸>醋酸 | D. | 开始,反应速率:盐酸>醋酸 |
分析 c(H+)相同的盐酸和醋酸,则两种溶液中氢离子浓度相等,反应速率和离子浓度成正比,醋酸是弱电解质,氯化氢是强电解质,所以C(HCl)<C(CH3COOH),若最后锌粒全部溶解且放出气体一样多,可能是盐酸恰好反应而醋酸过量,也可能是盐酸和醋酸都过量,以此解答该题.
解答 解:A.醋酸是弱酸,随反应的进行会不断电离出氢离子,所以氢离子浓度有增大的趋势,所以整个阶段的平均速率:醋酸>盐酸,故A正确;
B.反应过程中,醋酸电离导致醋酸中氢离子浓度减少速率小于盐酸中氢离子浓度减少速率,盐酸中的氢离子浓度小于醋酸中氢离子浓度,盐酸反应速率小于醋酸,所以反应所需时间:盐酸>醋酸,故B错误;
C.参加反应的锌的质量和生成的氢气的量有关,因为产生气体体积相同,所以参加反应的锌的质量:醋酸=盐酸,故C错误;
D.pH相同的盐酸和醋酸,两种溶液中氢离子浓度相等,所以开始反应速率相等,故D错误.
故选A.
点评 本题考查弱电解质的电离,结合影响化学反应速率的因素综合考查学生的分析能力,为高频考点,注意把握弱电解质的电离特点,难度不大.

练习册系列答案
 天天向上口算本系列答案
天天向上口算本系列答案
相关题目
7.25℃时,若10mL pH=a的盐酸与100mL pH=b的Ba(OH)2溶液恰好完全反应,则a+b的值为( )
| A. | 14 | B. | 15 | C. | 13 | D. | 无法确定 |
1.对比以下几个反应式:
Cl+Cl→Cl2△H1=-243kJ/mol;
O+O→O2△H2=-497kJ/mol;
N+N→N2△H3=-946kJ/mol.
你可以得出的结论是( )
Cl+Cl→Cl2△H1=-243kJ/mol;
O+O→O2△H2=-497kJ/mol;
N+N→N2△H3=-946kJ/mol.
你可以得出的结论是( )
| A. | 在常温下氮气比氧气和氯气稳定 | |
| B. | 氮、氧和氯的单质常温下为气体 | |
| C. | 氮、氧和氯分子在反应过程中释放能量 | |
| D. | 氮气、氧气和氯气的密度不同 |
18.下列叙述正确的是( )
| A. | 组成元素相同,各元素质量分数也相同的不同物质属于同系物 | |
| B. | 分子式相同的不同物质一定是同分异构体 | |
| C. | 相对分子质量相同的不同物质一定是同分异构体 | |
| D. | 通式相同的不同物质一定属于同系物 |
15.下列哪项成果获得2016年诺贝尔化学奖( )
| A. | 中国科学家屠呦呦成功提取出青蒿素用于治疗疟疾,挽救许人的生命 | |
| B. | 法国的让彼埃尔索瓦等三位科学家成功研制出分子机器 | |
| C. | 美国的三位科学家在拓扑相变领域的突出贡献 | |
| D. | 中国科学家蔡启瑞院士非酶催化剂合成氨以及化学方面突碳一出贡献 |
2.下列事实与胶体性质有关的是( )
①豆浆加入盐卤做豆腐 ②在河流入海口易形成沙洲 ③油水混合会分层④工厂采用静电除尘 ⑤CuSO4与NaOH溶液混合产生沉淀 ⑥血液透析.
①豆浆加入盐卤做豆腐 ②在河流入海口易形成沙洲 ③油水混合会分层④工厂采用静电除尘 ⑤CuSO4与NaOH溶液混合产生沉淀 ⑥血液透析.
| A. | ①②④⑥ | B. | ①②③⑤ | C. | ③④⑤⑥ | D. | 全部 |
19.工业上通常采用CO(g)和H2(g)催化合成甲醇CH3OH(g).
(1)在一定温度和压强下,CO(g)+2H2(g)?CH3OH(g)△H=-128.8kJ/mol.若将10a mol CO和20a mol H2放入2L的密闭容器中,充分反应后测得CO的转化率为60%,则该反应的平衡常数为$\frac{3}{32{a}^{2}}$(用含a的代数式表示).
若此时再向该容器中投入10a mol CO、20a mol H2和10a mol CH3OH(g),判断平衡移动的方向是正向移动(填“正向移动”、“逆向移动”或“不移动”);
与原平衡相比,CO的物质的量浓度增大(填“增大”、“不变”或“减小”).
(2)判断该反应达到平衡状态的依据是BE(填字母序号).
A.混合气体的密度不变
B.混合气体的平均相对分子质量不变
C.2v逆(H2)=v正(CO)
D.容器内CO、H2、CH3OH的浓度之比为1:2:1
E.CH3OH、CO、H2的浓度都不再发生变化
(3)一定条件下,在容积相同的三个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如表:
则a+b=128.8;α1+α3<1(填“<”、“>”或“=”,).
(1)在一定温度和压强下,CO(g)+2H2(g)?CH3OH(g)△H=-128.8kJ/mol.若将10a mol CO和20a mol H2放入2L的密闭容器中,充分反应后测得CO的转化率为60%,则该反应的平衡常数为$\frac{3}{32{a}^{2}}$(用含a的代数式表示).
若此时再向该容器中投入10a mol CO、20a mol H2和10a mol CH3OH(g),判断平衡移动的方向是正向移动(填“正向移动”、“逆向移动”或“不移动”);
与原平衡相比,CO的物质的量浓度增大(填“增大”、“不变”或“减小”).
(2)判断该反应达到平衡状态的依据是BE(填字母序号).
A.混合气体的密度不变
B.混合气体的平均相对分子质量不变
C.2v逆(H2)=v正(CO)
D.容器内CO、H2、CH3OH的浓度之比为1:2:1
E.CH3OH、CO、H2的浓度都不再发生变化
(3)一定条件下,在容积相同的三个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如表:
| 容器 | 甲 | 乙 | 丙 | |
| 反应物投入量 | 1 mol CO、 2 mol H2 | 1 mol CH3OH | 2 mol CH3OH | |
| 平衡 时数 据 | 反应能量变化的绝对值(kJ) | a | b | c |
| 反应物转化率 | α1 | α2 | α3 | |
20.某反应过程能量变化如图所示,下列说法正确的是( )
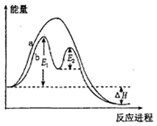

| A. | 反应过程a有催化剂参与 | |
| B. | 该反应为吸热反应 | |
| C. | 改变催化剂,可改变该反应的活化能 | |
| D. | 有催化剂条件下,反应的活化能等于E1+E2 |