题目内容
20.某元素R在自然界只存在两种天然同位素,且它们的含量相近,R的相对原子质量为152,原子核外的电子数为63.下列关于R的叙述中错误的是( )| A. | R不是主族元素 | B. | R是第六周期元素 | ||
| C. | R的原子核内有63个质子 | D. | R的一种同位素的核内有89个中子 |
分析 已知元素R在自然界存在同位素,所以R的相对原子质量为平均相对原子质量,不能代表各同位素的相对原子质量,也不能代表各同位素的质量数,因此中子数不能计算出来,根据原子核外的电子数等于核内质子数(原子序数),再来确定R所在周期表中的位置.
解答 解:A.因核外电子数等于其质子数为63,用质子数分别减去各周期所含有的元素种类,63-2-8-8-18-18=9,显然其属于第六周期,从左到右的第9种,而第六周期中包含镧系,所以它应属于副族,故A正确;
B.因核外电子数等于其质子数为63,用质子数分别减去各周期所含有的元素种类,63-2-8-8-18-18=9,显然其属于第六周期,故B正确;
C.核外电子数等于其质子数,故C正确;
D.同种元素的不同核素质量数不同,不能用元素的相对原子质量代表某种核素的质量数,故D错误;
故选D.
点评 本题需要掌握根据原子序数推知元素在周期表中的位置,熟悉元素周期表的结构,这是解题的关键.

练习册系列答案
 红果子三级测试卷系列答案
红果子三级测试卷系列答案 课堂练加测系列答案
课堂练加测系列答案
相关题目
8.下列各组物质熔化或升华时,所克服的粒子间作用属于同种类型的是( )
| A. | 碘和干冰升华 | B. | 镁和硫熔化 | ||
| C. | 氯化钠和蔗糖熔化 | D. | Na2O和SiO2熔化 |
15.有8种物质:①甲烷;②苯;③聚乙烯;④聚1,3-丁二烯;⑤2-丁炔;⑥环己烷;⑦邻二甲苯;⑧环己烯.既能使酸性高锰酸钾溶液褪色又能与溴水反应使之褪色的是( )
| A. | ③④⑤⑧ | B. | ④⑤⑧ | C. | ④⑤⑦⑧ | D. | ③④⑤⑦⑧ |
12.下列关于化学反应的描述中正确的是( )
| A. | 当一个化学反应在一定条件下达到最大限度时,反应速率也最大 | |
| B. | 用一定量的锌片和足量的稀硫酸反应制氢气时,加入少量氧化铜,可以加快反应的速率且生成氢气的总量不变 | |
| C. | 燃烧一定是放热反应,也是氧化还原反应 | |
| D. | 化学反应中能量变化的大小与反应物的状态无关 |
10.化学与生产、生活密切相关,下列说法正确的是( )
| A. | 淀粉、纤维素都属天然高分子化合物 | |
| B. | 食品包装袋中可用碱石灰做干燥剂 | |
| C. | 煤经过液化等物理变化可转化为清洁燃料 | |
| D. | 制作航天服的聚醋纤维属新型无机非金属材料 |
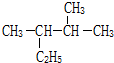 的系统命名为2,3-二甲基戊烷.
的系统命名为2,3-二甲基戊烷.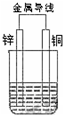 如图所示原电池
如图所示原电池