题目内容
10.化学与生产、生活密切相关,下列说法正确的是( )| A. | 淀粉、纤维素都属天然高分子化合物 | |
| B. | 食品包装袋中可用碱石灰做干燥剂 | |
| C. | 煤经过液化等物理变化可转化为清洁燃料 | |
| D. | 制作航天服的聚醋纤维属新型无机非金属材料 |
分析 A.从高分子化合物的定义角度分析;
B.碱石灰为氢氧化钠与氧化钙的混合物,吸收空气中的二氧化碳和水,但不能作为食品的干燥剂;
C.煤经过气化和液化都是化学变化;
D.制作航天服的聚醋纤维属有机高分子材料;
解答 解:A.淀粉、纤维素都属天然高分子化合物,故A正确;
B.碱石灰为氢氧化钠与氧化钙的混合物,吸收空气中的二氧化碳和水,但不能作为食品的干燥剂,故B错误;
C.煤经过气化生成水煤气,液化生成甲醇,都是化学变化,故C错误;
D. 制作航天服的聚醋纤维属有机高分子材料,故D错误;
故选A.
点评 本题考查较为综合,侧重于化学与生活、生产的考查,有利于培养学生的良好的科学素养,提高学生学习的积极性,题目难度不大,注意相关基础知识的积累.

练习册系列答案
相关题目
20.某元素R在自然界只存在两种天然同位素,且它们的含量相近,R的相对原子质量为152,原子核外的电子数为63.下列关于R的叙述中错误的是( )
| A. | R不是主族元素 | B. | R是第六周期元素 | ||
| C. | R的原子核内有63个质子 | D. | R的一种同位素的核内有89个中子 |
1.下列是除去括号内杂质的有关操作,其中正确的是( )
| A. | CO2(CO):通O2,点燃 | B. | CO(CO2):通过NaOH溶液 | ||
| C. | N2(O2):通过灼热的CuO | D. | CaO(CaCO3):加水,再过滤 |
18.下列关于化学反应速率的说法正确的是( )
| A. | 因是同一反应,所以用不同物质表示化学反应速率时,所得数值是相同的 | |
| B. | 根据化学反应速率的大小可以知道化学反应进行的快慢 | |
| C. | 化学反应速率为“1 mol/(L•min)”表示的意思是:时间为1 min 时,某物质的浓度为1 mol/L | |
| D. | 化学反应速率是指一定时间内任何一种反应物浓度的减少或者任何一种生成物浓度的增加 |
19.硫酸锌和轻质氧化镁在工业生产及食品添加等领域有重要应用.用高镁菱锌矿(主要含ZnCO3、MgCO3、CaCO3以及少量SiO2、Fe2O3、Cu等)进行联合生产.流程如图1:
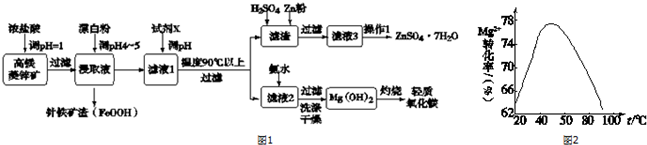
已知:金属离子沉淀的pH
(1)写出浸取过程中产生Fe2+的离子方程式Fe2O3+6H+=2Fe3++3H2O、2Fe3++Cu=2Fe2++Cu2+.
(2)下列说法正确的是acd.
a.用浓盐酸浸取前,将矿石粉碎能够提高浸出速率.
b.试剂X可以选择氨水,pH的范围在8.2~12.4之间.
c.控制温度在90℃以上的目的是为了促进Zn2+的水解.
d.滤渣中加入硫酸后再加入锌粉是为了出去Cu2+.
(3)由Fe2+生成针铁矿渣的离子反应方程式2Fe2++ClO-+3H2O=2FeOOH+Cl-+4H+.
(4)从滤液3中获取ZnSO4•7H2O的操作1是加热浓缩、冷却结晶、过滤、洗涤、干燥.
(5)加入氨水制备氢氧化镁的工艺过程要选择适宜条件.图2为反应温度与Mg2+转化率的关系.
①根据图中所示45℃前温度与Mg2+转化率之间的关系,可判断此反应是吸热(填“吸热”或“放热”)反应.
②50℃以上温度升高,Mg2+转化率下降的原因可能是温度过高时,氨水受热分解,浓度降低,Mg2+转化率下降.
③为了获取副产品CaCl2,经常用石灰乳代替氨水来制备氢氧化镁.用平衡移动原理解释石灰乳能够制备氢氧化镁的原因石灰乳中存在Ca(OH)2(s)?Ca2+(aq)+2OH-(aq),Mg2+可以与OH-反应生成更难溶的Mg(OH)2,使得OH-浓度不断下降,平衡右移,最终从Ca(OH)2转化为Mg(OH)2.

已知:金属离子沉淀的pH
| Zn2+ | Mg2+ | Cu2+ | Fe3+ | Fe2+ | |
| 开始沉淀pH | 5.9 | 9.4 | 4.7 | 2.7 | 7.6 |
| 完全沉淀pH | 8.2 | 12.4 | 6.7 | 3.7 | 9.6 |
(2)下列说法正确的是acd.
a.用浓盐酸浸取前,将矿石粉碎能够提高浸出速率.
b.试剂X可以选择氨水,pH的范围在8.2~12.4之间.
c.控制温度在90℃以上的目的是为了促进Zn2+的水解.
d.滤渣中加入硫酸后再加入锌粉是为了出去Cu2+.
(3)由Fe2+生成针铁矿渣的离子反应方程式2Fe2++ClO-+3H2O=2FeOOH+Cl-+4H+.
(4)从滤液3中获取ZnSO4•7H2O的操作1是加热浓缩、冷却结晶、过滤、洗涤、干燥.
(5)加入氨水制备氢氧化镁的工艺过程要选择适宜条件.图2为反应温度与Mg2+转化率的关系.
①根据图中所示45℃前温度与Mg2+转化率之间的关系,可判断此反应是吸热(填“吸热”或“放热”)反应.
②50℃以上温度升高,Mg2+转化率下降的原因可能是温度过高时,氨水受热分解,浓度降低,Mg2+转化率下降.
③为了获取副产品CaCl2,经常用石灰乳代替氨水来制备氢氧化镁.用平衡移动原理解释石灰乳能够制备氢氧化镁的原因石灰乳中存在Ca(OH)2(s)?Ca2+(aq)+2OH-(aq),Mg2+可以与OH-反应生成更难溶的Mg(OH)2,使得OH-浓度不断下降,平衡右移,最终从Ca(OH)2转化为Mg(OH)2.
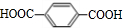
20.T℃时,AgCl在水溶液中的沉淀溶解平衡曲线如图所示.在该温度下,下列说法中不正确的是( )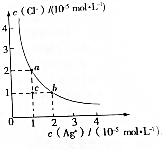

| A. | a点和b点对应的Ksp(AgCl)相等 | |
| B. | Ksp(AgCl)=2×10-10 | |
| C. | 可采取蒸发溶剂的方法使溶液从c点变到b点 | |
| D. | 已知Ksp(AgI)=8.5×10-17,向含KI和KCl的溶液中滴加AgNO3溶液,当AgCl开始沉淀时,溶液中$\frac{c({I}^{-})}{c(C{l}^{-})}$=4.25×10-7 |
 +2NaHCO3→
+2NaHCO3→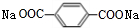 +2H2O+2CO2↑.
+2H2O+2CO2↑.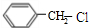 .
.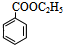 +H2O$→_{△}^{稀硫酸}$
+H2O$→_{△}^{稀硫酸}$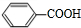 +CH3CH2OH.
+CH3CH2OH.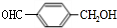 ,F与氢气1:1加成的芳香产物G中有3种氢,G与B发生聚合反应的化学方程式是n
,F与氢气1:1加成的芳香产物G中有3种氢,G与B发生聚合反应的化学方程式是n $\stackrel{一定条件下}{→}$
$\stackrel{一定条件下}{→}$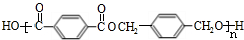 +(2n-1)H2O.
+(2n-1)H2O.