题目内容
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A、1 mol Cl2与足量的铁反应,转移的电子数为2NA |
| B、在含Al3+总数为NA的AlCl3溶液中,Cl-总数为3NA |
| C、在熔融状态下,1 mol NaHSO4完全电离出的阳离子数目为2NA |
| D、将0.1 mol NaCl全部溶于乙醇中制成胶体,其中含有的胶体粒子数目为0.1 NA |
考点:阿伏加德罗常数
专题:
分析:A.无论氯气是否过量,Fe在Cl2中燃烧都生成FeCl3,根据氯气计算转移电子数;
B.AlCl3是强酸弱碱盐,Al3+水解、Cl-不水解,所以溶液中Al3+、Cl-个数之比小于1:3;
C.熔融状态下,NaHSO4电离方程式为NaHSO4=Na++HSO4-,据此计算阳离子数目;
D.胶体粒子是多个微粒的集合体.
B.AlCl3是强酸弱碱盐,Al3+水解、Cl-不水解,所以溶液中Al3+、Cl-个数之比小于1:3;
C.熔融状态下,NaHSO4电离方程式为NaHSO4=Na++HSO4-,据此计算阳离子数目;
D.胶体粒子是多个微粒的集合体.
解答:
解:A.无论氯气是否过量,Fe在Cl2中燃烧都生成FeCl3,生成物与氯气的量无关,1mol氯气完全反应转移电子数为2NA,故A正确;
B.AlCl3是强酸弱碱盐,Al3+水解、Cl-不水解,所以溶液中Al3+、Cl-个数之比小于1:3,则在含Al3+总数为NA的AlCl3溶液中,Cl-总数大于3NA,故B错误;
C.熔融状态下,NaHSO4电离方程式为NaHSO4=Na++HSO4-,所以1molNaHSO4在熔融状态下电离出1mol阳离子,故C错误;
D.胶体粒子是多个微粒的集合体,所以无法计算胶体粒子个数,故D错误;
故选A.
B.AlCl3是强酸弱碱盐,Al3+水解、Cl-不水解,所以溶液中Al3+、Cl-个数之比小于1:3,则在含Al3+总数为NA的AlCl3溶液中,Cl-总数大于3NA,故B错误;
C.熔融状态下,NaHSO4电离方程式为NaHSO4=Na++HSO4-,所以1molNaHSO4在熔融状态下电离出1mol阳离子,故C错误;
D.胶体粒子是多个微粒的集合体,所以无法计算胶体粒子个数,故D错误;
故选A.
点评:本题考查阿伏伽德罗常数计算,涉及氧化还原反应、盐类水解、电解质的电离等知识点,注意硫酸氢钠在水溶液里和熔融状态下电离方程式的区别,为易错点.

练习册系列答案
相关题目
铜有两种常见的氧化物CuO和Cu2O.某学习小组取0.98g(用精密天平测量)Cu(OH)2固体加热,有铜的氧化物生成,其质量随温度变化如图1所示:另外,某同学绘制了三条表示金属氧化物与其所含金属元素的质量的关系曲线,如图2所示.则下列分析正确的是( )
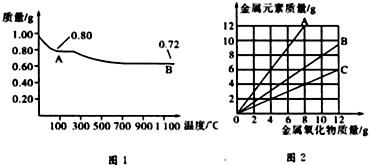

| A、图1中,A到B的过程中有0.01 mol电子发生了转移 |
| B、图1整个过程中共生成0.26 g水 |
| C、图2三条曲线中,表示CuO和其中所含Cu元素质量关系的曲线是A |
| D、图1中A和B化学式分别为Cu2O和CuO |
若NA表示阿伏加德罗常数的数值,下列叙述中不正确的是( )
| A、16g O2与O3混合物中所含电子数为8NA |
| B、标准状况下,2.24LCH3OH分子中共用电子对数为0.5NA |
| C、6gSiO2晶体中硅氧共价键数为0.4NA |
| D、0.1mol13C18O中所含中子数为1.7NA |
下列金属中,不能从硫酸铜溶液里置换出铜的是( )
| A、Al | B、Zn | C、Fe | D、Na |
反应Cl2+H2O=HCl+HClO中,水的作用是( )
| A、作氧化剂 |
| B、作还原剂 |
| C、既是氧化剂又是还原剂 |
| D、既不是氧化剂也不是还原剂 |
 请用如图的装置设计一个实验,以测定SO2转化为SO3的转化率.
请用如图的装置设计一个实验,以测定SO2转化为SO3的转化率.