题目内容
20.将一定质量的铁、氧化铁、氧化铜的混合物粉末放入100mL4.40mol/L盐酸中,充分反应后产生896mLH2(标准状况),残留固体1.28g.过滤,滤液中无Cu2+.将滤液加水稀释到200mL,测得其中c(H+)为0.400mol/L.求原混合物中单质铁的质量.分析 滤液中没有Cu2+,说明溶液中也没有Fe3+,则溶液中阳离子有Fe2+和H+,溶质为FeCl2和HCl,
根据电荷守恒得2n(Fe2+)+n(H+)=n(Cl-),则n(Fe2+)=$\frac{4.40mol/L×0.1L-0.40mol/L×0.2L}{2}$mol=0.18mol,生成n(H2)=$\frac{0.896L}{22.4L/mol}$=0.04mol,因为还有盐酸剩余,溶液残留固体是Cu,n(Cu)=$\frac{1.28g/mol}{64g/mol}$=0.02mol,
设Fe的物质的量为xmol、Fe2O3的物质的量为ymol,根据Fe原子守恒得:x+2y=0.18,根据转移电子守恒得2x=0.04×2+0.02×2+2y×1,从而计算n(Fe),根据m=nM计算铁的质量.
解答 解:完全反应后滤液中没有Cu2+,说明溶液中也没有Fe3+,则溶液中阳离子有Fe2+和H+,溶质为FeCl2和HCl,
根据电荷守恒得2n(Fe2+)+n(H+)=n(Cl-),则n(Fe2+)=$\frac{4.40mol/L×0.1L-0.40mol/L×0.2L}{2}$mol=0.18mol,生成n(H2)=$\frac{0.896L}{22.4L/mol}$=0.04mol,因为还有盐酸剩余,溶液残留固体是Cu,n(Cu)=$\frac{1.28g/mol}{64g/mol}$=0.02mol,
设Fe的物质的量为xmol、Fe2O3的物质的量为ymol,
根据Fe原子守恒得:x+2y=0.18
根据转移电子守恒得:2x=0.04×2+0.02×2+2y×1,
解得:x=0.10、y=0.04,
所以原混合物中铁的质量为:m(Fe)=0.10mol×56g/mol=5.6g,
答:原混合物中单质铁的质量为5.6g.
点评 本题考查混合物反应的计算,题目难度中等,试题侧重考查分析计算能力,明确溶液中的溶质是解本题关键,注意掌握守恒思想在化学计算中的应用方法,试题培养了学生的化学计算能力.

| A. | 二氧化硅和氯化镁熔化 | B. | 碘和氯化铵受热变成气体 | ||
| C. | 碘和干冰的升华 | D. | 氯化钠和氯化氢溶于水 | ||
| E. | 硅和蔗糖的熔化 | F. | 酒精和水的挥发 |
| A. | ①②④⑤ | B. | ②④⑤⑥ | C. | ②③④⑤ | D. | 全部 |
| A. | 0.1mol/L | B. | 0.2mol/L | C. | 0.4mol/L | D. | 0.8mol/L |
| A. | Cu $\stackrel{稀HNO_{3}}{→}$Cu(NO3)2 | |
| B. | Cu $\stackrel{Cl_{2}}{→}$CuCl2 $\stackrel{NaOH溶液}{→}$Cu(OH)2 $\stackrel{稀HNO_{3}}{→}$ Cu(NO3)2 | |
| C. | Cu $\stackrel{O_{2}}{→}$CuO$\stackrel{稀HNO_{3}}{→}$ Cu(NO3)2 | |
| D. | Cu $\stackrel{浓H_{2}SO_{4}}{→}$CuSO4 $\stackrel{Ba(NO_{3})_{2}溶液}{→}$ Cu(NO3)2 |
废液$→_{①}^{提纯、结晶}$FeSO4•7HO2$\stackrel{②}{→}$FeSO4溶液$→_{③}^{NH_{4}HCO_{3}溶液}$FeCO3$\stackrel{④}{→}$Fe2CO3
已知步骤①中硫酸亚铁在不同温度下的溶解度和析出晶体的组成如下表所示.
| 温度/℃ | 0 | 10 | 30 | 50 | 56.7 | 60 | 64 | 70 | 80 | 90 | ||
| 溶解度/g | 14.0 | 17.0 | 25.0 | 33.0 | 35.2 | 35.3 | 35.6 | 33.0 | 30.5 | 27.0 | ||
| 析出晶体 | FeSO4•7H2O | FeSO4•4H2O | FeSO4•H2O | |||||||||
(1)步骤②需加一定量硫酸,其主要目的是抑制FeSO4的水解;
(2)生产FeCO3浊液的离子方程式为Fe2++2HCO3-═FeCO3↓+CO2↑+H2O;
(3)FeCO3浊液露置在空气中会出现红褐色的固体,该变化的化学方程式为4FeCO3+6H2O+O2═4Fe(OH)3+4CO2;
(4)已知FeSO4•7H2O晶体在加热条件下发生反应,其中一种生成物会用于涂料中的着色剂.请写出
FeSO4•7H2O分解的反应式FeSO4•7H2O$\frac{\underline{\;高温\;}}{\;}$Fe2O3+SO2↑+SO3↑+14H2O↑;利用如图装置可检验该反应的气体产物.
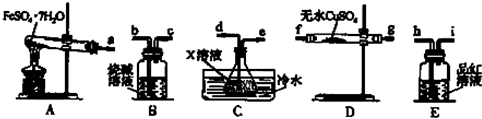
请填写下列空白:
①仪器的连接顺序为a 接f(或g)、g(或f)接d、e接h、i接b;
②装置C中的X为氯化钡溶液.
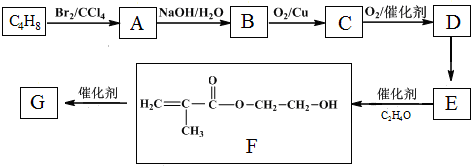
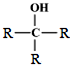 $\stackrel{O_{2}/Cu}{→}$不能被氧化
$\stackrel{O_{2}/Cu}{→}$不能被氧化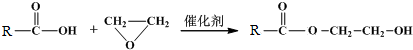
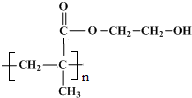 .
.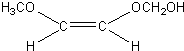 、
、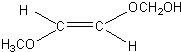 、
、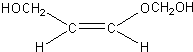 、
、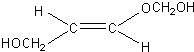 .
.