题目内容
20.质量反应的离子方程式书写正确的是( )| A. | 氢氧化镁与稀盐酸反应:H++OH-═H2O | |
| B. | 氯化钡溶液与硫酸钠溶液反应:Ba2++SO42-═BaSO4↓ | |
| C. | FeCl3溶液中加入Fe粉:Fe3++Fe═2Fe2+ | |
| D. | 碳酸钠溶液与足量醋酸反应:Na2CO3+2H+═2Na++CO2↑+H20 |
分析 A.氢氧化镁为难溶物质;
B.氯化钡溶液与硫酸钠溶液反应生成硫酸钡沉淀;
C.电荷不守恒;
D.醋酸为弱电解质,要写分子.
解答 解:A.氢氧化镁为难溶物质,则氢氧化镁与稀盐酸反应:2H++Mg(OH)2═Mg2++2H2O,故A错误;
B.氯化钡溶液与硫酸钠溶液反应生成硫酸钡沉淀,其反应的离子方程式为:Ba2++SO42-═BaSO4↓,故B正确;
C.FeCl3溶液中加入Fe粉:2Fe3++Fe═3Fe2+,故C错误;
D.碳酸钠溶液与足量醋酸反应:CO32-+2CH3COOH→2CH3COO-+CO2↑+H20,故D错误.
故选B.
点评 本题考查离子方程式的书写,侧重于学生的分析能力和元素化合物知识的综合运用的考查,注意把握离子的反应必须符合反应的实际,注意电荷守恒和质量守恒问题,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
11.依据元素周期律进行推断,下列不正确的是( )
| A. | 碱性:KOH>NaOH | B. | 氧化性:Cl2>S | C. | 稳定性:HBr>HI | D. | 酸性:H3PO4>HNO3 |
8.化学与社会、科学、技术、环保密切相关.下列有关说法不正确的是( )
| A. | 荧光蛋白是一种高分子化合物且能发生水解 | |
| B. | 用纯碱溶液和盐酸可以清洗锅炉中的硫酸钙 | |
| C. | 利用次氯酸钠溶液的碱性对餐具和环境消毒 | |
| D. | 大量排放PM2.5、SO2、NOX等会形成雾霾 |
15.同温同压下,相同质量的下列气体中,体积最大的是( )
| A. | N2 | B. | SO2 | C. | Cl2 | D. | CO2 |
5.(1)由于钠很容易与空气中的二氧化碳和水等物质反应,所以钠在自然界里只能以化合态存在.
(2)维生素C又称为抗坏血酸,在人体内有重要的功能.例如帮助人体将食物中摄取的不易吸收的Fe3+变为易吸收的Fe2+.这说明维生素C具有还原性(填氧化性或还原性).
(3)写出下列空格内物质的名称、俗名或化学式:
(4)写出下列电离方程式或化学方程式:①Na2CO3在水溶液中的电离方程式Na2CO3=2Na++CO32-②曾青(CuSO4)得铁化为铜的化学方程式Fe+CuSO4=Cu+FeSO4.
(2)维生素C又称为抗坏血酸,在人体内有重要的功能.例如帮助人体将食物中摄取的不易吸收的Fe3+变为易吸收的Fe2+.这说明维生素C具有还原性(填氧化性或还原性).
(3)写出下列空格内物质的名称、俗名或化学式:
| 名称 | 氧化铁 | 碳酸钠 | 碳酸氢钠 |
| 俗名 | 铁红 | 小苏打 | |
| 化学式 | Na2CO3 | NaHCO3 |
9.用NA表示阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 常温常压下的33.6 L氯气与27 g铝充分反应,转移电子数为3NA | |
| B. | 常温下,46 g分子式为C2H6O的物质中一定含有极性键为7NA,非极性键为NA | |
| C. | 125 mL 16 mol/L浓硫酸与足量的铜反应,生成SO2的分子数小于NA | |
| D. | 标准状况下,体积为22.4 L NO2、N2O4的混合气体,升温至常温,则混合气体分子数为NA |
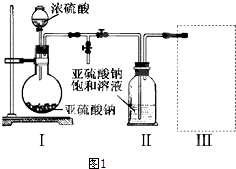
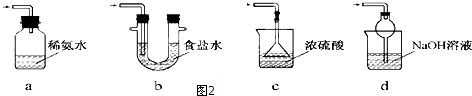

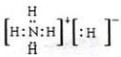 .
.