题目内容
 (1)如图是维生素A的分子结构:
(1)如图是维生素A的分子结构:维生素A中的含氧官能团是
(2)对于CH4、C2H2、C2H4、C2H6、C3H6五种烃,请回答:
①等质量的五种烃,在相同状况下所占体积最大的是
②等质量的五种烃,完全燃烧时消耗O2最多的是
③在120℃、101.3kPa时,与足量的氧气完全燃烧时,反应后气体体积减小的是
考点:有机物的结构和性质,化学方程式的有关计算,有机物分子中的官能团及其结构
专题:有机物的化学性质及推断,烃及其衍生物的燃烧规律
分析:(1)根据结构简式来寻找官能团以及书写有机物的分子式,有机物中含有-OH和C=C;碳碳双键可以和溴水发生加成反应;
(2)①根据n=
,V=nVm可知,相同条件下,质量相同时,气体的相对分子质量越小,气体所占体积越大;
②质量相同时,分子中H元素的质量分数越大,完全燃烧时消耗O2越多;
③120℃,水为气体,利用燃烧的化学方程式,借助化学计量数判断体积的变化.
(2)①根据n=
| m |
| M |
②质量相同时,分子中H元素的质量分数越大,完全燃烧时消耗O2越多;
③120℃,水为气体,利用燃烧的化学方程式,借助化学计量数判断体积的变化.
解答:
解:(1)根据维生素A的结构简式可以看出有机物中含有-OH和C=C,名称为羟基、碳碳双键,含氧官能团是羟基(-OH),分子式为C20H30O,
1mol维生素A中含有碳碳双键5mol,碳碳双键可以和溴发生加成反应,所以1mol维生素A最多能与5mol溴发生加成反应,
故答案为:羟基(-OH);C20H30O;5;
(2)①CH4、C2H4、C2H2、C2H6、C3H6的相对分子质量大小为:CH4<C2H2<C2H4<C2H6<C3H6,根据n=
,V=nVm可知,相同条件下,质量相同时,气体的相对分子质量越小,气体所占体积越大,则质量相同时,在相同状况下体积最大的是CH4,故答案为:CH4;
②CH4、C2H4、C2H2、C2H6、C3H6的H%大小为:CH4>C2H6>C3H6=C2H4>C2H2,质量相同时,分子中H元素的质量分数越大,完全燃烧时消耗O2越多,故完全燃烧时消耗O2的量最多的是CH4,故答案为:CH4;
③CH4+2O2
CO2+2H2O
C2H4+3O2
2CO2+2H2O
C2H2+2.5O2
2CO2+H2O
C2H6+3.5O2
2CO2+3H2O
C3H6+4.5O2
3CO2+3H2O,
由上面的化学方程式可以看出气体体积不变的是甲烷和乙烯,
气体体积增大的是C2H6、C3H6,
气体体积减小的是C2H2,故答案为:C2H2.
1mol维生素A中含有碳碳双键5mol,碳碳双键可以和溴发生加成反应,所以1mol维生素A最多能与5mol溴发生加成反应,
故答案为:羟基(-OH);C20H30O;5;
(2)①CH4、C2H4、C2H2、C2H6、C3H6的相对分子质量大小为:CH4<C2H2<C2H4<C2H6<C3H6,根据n=
| m |
| M |
②CH4、C2H4、C2H2、C2H6、C3H6的H%大小为:CH4>C2H6>C3H6=C2H4>C2H2,质量相同时,分子中H元素的质量分数越大,完全燃烧时消耗O2越多,故完全燃烧时消耗O2的量最多的是CH4,故答案为:CH4;
③CH4+2O2
| 点燃 |
C2H4+3O2
| 点燃 |
C2H2+2.5O2
| 点燃 |
C2H6+3.5O2
| 点燃 |
C3H6+4.5O2
| 点燃 |
由上面的化学方程式可以看出气体体积不变的是甲烷和乙烯,
气体体积增大的是C2H6、C3H6,
气体体积减小的是C2H2,故答案为:C2H2.
点评:本题考查有机物结构性质及计算,为高频考点,把握有机物的燃烧的计算和判断、有机物的组成特点为解答的关键,注重基础知识的考查,题目难度不大.

练习册系列答案
 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案
相关题目
分子式为C6H14O的醇有多种结构,期中能经过两步氧化生成羧酸的结构有(不考虑立体异构)( )
| A、7种 | B、8种 | C、9种 | D、10种 |
下列说法中正确的是( )
| A、氦分子中含有共价键 |
| B、含有共价键的化合物一定是共价共价化合物 |
| C、离子化合物中可能含有极性共价键或非极性共价键 |
| D、同一元素的各种同位素的物理性质、化学性质均相同 |
下列说法不正确的是( )
| A、利用太阳能在催化剂参与下分解水制氢是把光能转化为化学能的绿色化学 |
| B、蔗糖、淀粉、油脂及其水解产物均为非电解质 |
| C、通过红外光谱分析可以区分乙醇和乙酸乙酯 |
| D、米饭的主要成分是淀粉 |




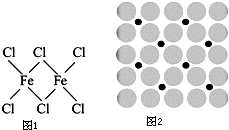 铁及铁的化合物在生产、生活中有广泛应用.请回答下列问题:
铁及铁的化合物在生产、生活中有广泛应用.请回答下列问题:

 甲是生产某新型工程塑料的基础原料之一,由C、H、O三种元素组成,其分子结构模型如图所示(图中球与球之间连线代表化学键单键或双键),根据分子结构模型
甲是生产某新型工程塑料的基础原料之一,由C、H、O三种元素组成,其分子结构模型如图所示(图中球与球之间连线代表化学键单键或双键),根据分子结构模型