题目内容
美籍埃及人泽维尔用激光闪烁照相机拍摄到化学反应中化学键断裂和形成的过程,因而获得1999年诺贝尔化学奖.激光有很多用途,例如波长为10.3 微米的红外激光能切断B(CH3)3分子中的一个B-C键,使之与HBr发生取代反应:B(CH3)3+HBr→B(CH3)2Br+CH4而利用9.6微米的红外激光却能切断两个B-C键,并与HBr发生二元取代反应.
(1)试写出二元取代的化学方程式:
(2)利用5.6g B(CH3)3和9.72g HBr正好完全反应,则生成物中甲烷的物质的量为 ,其他两种产物的物质的量之比为 .
(1)试写出二元取代的化学方程式:
(2)利用5.6g B(CH3)3和9.72g HBr正好完全反应,则生成物中甲烷的物质的量为
考点:化学方程式的有关计算
专题:计算题
分析:(1)由反应信息可知,B(CH3)3分子中的一个B-C键断裂,Br原子取代甲基,甲基与H原子结合生成甲烷,故B(CH3)3和HBr反应生成其二溴代物为B(CH3)Br2,1molB(CH3)3发生二溴取代同时生成2mol甲烷;
(2)根据n=
计算5.6g B(CH3)3和9.72g HBr的物质的量,假设生成的B(CH3)2Br为xmol,生成B(CH3)Br2为ymol,结合B原子及溴原子守恒列方程计算,根据C原子守恒计算甲烷的物质的量.
(2)根据n=
| m |
| M |
解答:
解:(1)由反应信息可知,B(CH3)3分子中的一个B-C键断裂,Br原子取代甲基,甲基与H原子结合生成甲烷,B(CH3)3和HBr反应生成其二溴代物为B(CH3)Br2,1molB(CH3)3发生二溴取代同时生成2mol甲烷,反应方程式为:B(CH3)Br2+2HBr
B(CH3)Br2+2CH4,
故答案为:B(CH3)Br2+2HBr
B(CH3)Br2+2CH4;
(2)5.6g B(CH3)3的物质的量为
=0.1mol,9.72g HBr的物质的量为
=0.12mol,
假设生成的B(CH3)2Br为xmol,生成B(CH3)Br2为ymol,根据B原子及溴原子守恒,则:
解得:x=0.08,y=0.02,
故B(CH3)2Br与B(CH3)Br2的物质的量之比为:0.08mol:0.02mol=4:1,
由碳原子守恒可知,甲烷的物质的量=0.1mol×3-0.08mol×2-0.02mol=0.12mol,
答:0.12mol;n[B(CH3)2Br]:n[B(CH3) Br2]=4:1.
| 9.6微米红外激光 |
故答案为:B(CH3)Br2+2HBr
| 9.6微米红外激光 |
(2)5.6g B(CH3)3的物质的量为
| 5.6g |
| 56g/mol |
| 9.72g |
| 81g/mol |
假设生成的B(CH3)2Br为xmol,生成B(CH3)Br2为ymol,根据B原子及溴原子守恒,则:
|
解得:x=0.08,y=0.02,
故B(CH3)2Br与B(CH3)Br2的物质的量之比为:0.08mol:0.02mol=4:1,
由碳原子守恒可知,甲烷的物质的量=0.1mol×3-0.08mol×2-0.02mol=0.12mol,
答:0.12mol;n[B(CH3)2Br]:n[B(CH3) Br2]=4:1.
点评:本题考查根据方程式的计算,难度不大,理解发生取代反应的原理是解题的关键,注意根据守恒进行计算.

练习册系列答案
相关题目
可逆反应达到平衡的重要特征是( )
| A、反应停止了 |
| B、正、逆反应的速率相等 |
| C、反应物和生成物的浓度相等 |
| D、正、逆反应速率都为零 |
将a g Fe、Mg合金溶解在一定量的稀硝酸中,当合金完全溶解后,收集到标准状况下的NO气体b L(设HNO3的还原产物只有NO),再向反应后的溶液中加入足量NaOH溶液,得到沉淀物.若用守恒法求沉淀的质量,用到的守恒关系依次是( )
| A、质量守恒、电子守恒、电荷守恒 |
| B、电子守恒、质量守恒、电荷守恒 |
| C、电子守恒、电荷守恒、质量守恒 |
| D、电荷守恒、质量守恒、电子守恒 |
设NA为阿伏加德罗常数,下列说法正确的是( )
| A、32g O2气体含有的氧原子数为NA |
| B、2L 0.3mol/L Na2SO4溶液中含有Na+为0.6NA |
| C、27g铝完全反应后失去的电子数为3NA |
| D、11.2L氮气所含的分子数为0.5NA |
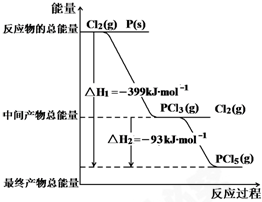 红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g).反应过程和能量关系如图所示( 图中的△H表示生成1mol产物的数据).根据图示,回答下列问题:
红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g).反应过程和能量关系如图所示( 图中的△H表示生成1mol产物的数据).根据图示,回答下列问题: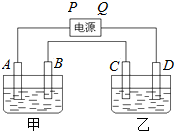 已知A、B、C、D都是铂电极,P、Q是直流电源的两极,通电后发现B极质量增加.
已知A、B、C、D都是铂电极,P、Q是直流电源的两极,通电后发现B极质量增加.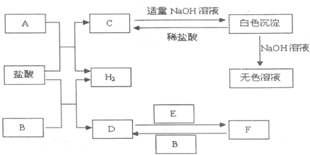 下列物质A~F是我们熟悉的单质或化合物,其中A、E均为C中元素形成的单质,B是常见的金属,且B的合金用量最大;在适当的条件下,它们之间可以发生如图所示的转化.
下列物质A~F是我们熟悉的单质或化合物,其中A、E均为C中元素形成的单质,B是常见的金属,且B的合金用量最大;在适当的条件下,它们之间可以发生如图所示的转化.