题目内容
设NA为阿伏加德罗常数,下列说法正确的是( )
| A、32g O2气体含有的氧原子数为NA |
| B、2L 0.3mol/L Na2SO4溶液中含有Na+为0.6NA |
| C、27g铝完全反应后失去的电子数为3NA |
| D、11.2L氮气所含的分子数为0.5NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.32g氧气的物质的量为1mol,1个氧气分子中含有2个氧原子;
B.2L 0.3mol/L Na2SO4溶液的物质的量为Na2SO4化学式计算钠离子的个数;
C.依据n=
计算物质的量,Al~Al3+,据此解答;
D.依据气体摩尔体积的条件应用分析判断.
B.2L 0.3mol/L Na2SO4溶液的物质的量为Na2SO4化学式计算钠离子的个数;
C.依据n=
| m |
| M |
D.依据气体摩尔体积的条件应用分析判断.
解答:
解:A.氧气的物质的量为:
=1mol,一个氧气分子含2个氧原子,所以氧原子的个数为1mol×2×NA=2NA,故A错误;
B.硫酸钠的物质的量为:2L×0.3mol/L=0.6mol,1mol硫酸钠电离产生2mol钠离子,所以钠离子的物质的量为0.6mol×2=1.2mol,Na+个数为1.2mol×NA=1.2NA,故B错误;
C.27g铝的物质的量为
=1mol,1mol铝失去3mol电子转化成铝离子,所以27g铝完全反应后失去的电子数为3×NA=3NA ,故C正确;
D.没指明标准状况下,Vm≠22.4L/mol,则11.2L氮气的物质的量不是0.5mol,则所含的分子数不一定为0.5NA,故D错误;
故选:C.
| 32g |
| 32g/mol |
B.硫酸钠的物质的量为:2L×0.3mol/L=0.6mol,1mol硫酸钠电离产生2mol钠离子,所以钠离子的物质的量为0.6mol×2=1.2mol,Na+个数为1.2mol×NA=1.2NA,故B错误;
C.27g铝的物质的量为
| 27g |
| 27g/mol |
D.没指明标准状况下,Vm≠22.4L/mol,则11.2L氮气的物质的量不是0.5mol,则所含的分子数不一定为0.5NA,故D错误;
故选:C.
点评:本题考查阿伏加德罗常数,题目难度不大,既要掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,还要准确弄清分子、原子、原子核内质子中子及核外电子的构成关系,注意气体摩尔体积使用的条件.

练习册系列答案
相关题目
下列物质中,含有极性键的离子化合物是( )
| A、KCl |
| B、H2O2 |
| C、Na2O2 |
| D、NaOH |
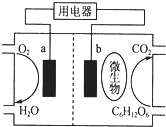 以葡萄糖为燃料的微生物燃料电池结构如图所示.a为电池的正极,关于该电池的叙述正确的是( )
以葡萄糖为燃料的微生物燃料电池结构如图所示.a为电池的正极,关于该电池的叙述正确的是( )| A、该电池能够在高温下工作 |
| B、b电极发生还原反应 |
| C、O2在a电极被氧化 |
| D、电流从a电极经用电器流向b电极 |
短周期中的A、B、C、D、E五种元素,原子序数依次增大.A和D,C和E分别同主族,A为非金属元素,且A与B的原子序数之和等于C的原子序数,C2-与D+的核外电子数相等.则下列说法正确的是( )
| A、B与A只能组成BA3化合物 |
| B、C、D、E形成的化合物水溶液可能显碱性 |
| C、A、B、C形成的化合物一定不能发生水解反应 |
| D、E的氧化物对应的水化物只具有氧化性 |
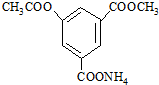 某有机物的结构简式如图所示,该物质1mol与足量NaOH溶液充分反应,消耗NaOH物质的量为( )
某有机物的结构简式如图所示,该物质1mol与足量NaOH溶液充分反应,消耗NaOH物质的量为( )| A、5mol | B、4mol |
| C、3mol | D、2mol |
下列有关碱金属元素性质的叙述中,正确的是( )
| A、碱金属的单质中,锂的还原性最强 |
| B、K与水反应最剧烈 |
| C、在自然界中它们无游离态存在 |
| D、单质的熔沸点依次升高 |