题目内容
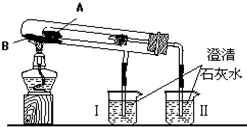
19.某化学小组利用如图装置进行某些气体的制备和性质实验,图中加持装置有省略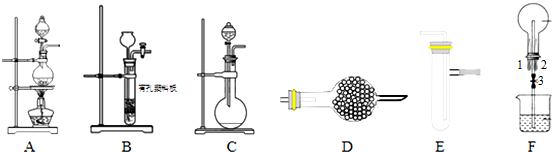
(1)为制取干燥氨气,可将装置C与装置D连接,则装置D中 的固体宜选用ad
a.碱石灰 b.无水氯化钙 c.五氧化二磷 d.生石灰
(2)装置A、E、E连接可制取纯净干燥的氯气,则两个E装置内的药品依次是饱和食盐水、浓硫酸
(3)装置F可用于探究氯气和氨气反应,实验室打开开关1、3,关闭2,先向烧瓶中通入氯气,然后关闭1、3,打开2,向烧瓶中缓慢通入一定量的另一种气体.实验一段时间后烧瓶内出现浓厚的白烟并在容器内壁凝结,请设计一个实验方案鉴定该固体中的阳离子取少量固体于试管中,加入适量NaOH溶液并加热,在管口用湿润的红色石蕊试纸检验产生的气体,若湿润的红色石蕊试纸变蓝,证明固体中有NH4+.
(4)利用装置A、E,可设计实验比较氯离子和溴离子的还原性强弱,能证明结论的实验现象是装置E中的NaBr溶液变橙红色.若利用装置A、E进行乙烯与溴水反应的实验,必须对装置A进行的改动是将分液漏斗改为温度计,并使温度计水银球没入烧瓶内液面下.
(5)将装置B、C分别于F相连后,进行硫化氢和二氧化硫反应的实验,烧杯中的试剂所起的作用是证明烧瓶中压强减少,同时吸收剩余气体二氧化硫或硫化氢有毒气体.
分析 (1)实验中干燥氨气可以用碱石灰或生石灰;
(2)依据制备氯气装置是利用二氧化锰和浓盐酸加热反应,生成的氯气中含有氯化氢和水蒸气,通过饱和食盐水除去氯化氢,通过浓硫酸除去水蒸气;
(3)实验时打开开关1、3,关闭2向烧瓶中通入氯气,然后关闭1、3,打开2,向烧瓶中缓慢通入一定量的氨气,实验一段时间后烧瓶内出现浓厚的白烟并在容器内壁凝结,依据反应化学方程式判断是生成的氯化氢和氨气反应生成的氯化铵;依据铵根离子的检验方法是和碱反应生成氨气设计实验检验;
(4)利用装置A、E,可设计实验比较Cl-和Br-的还原性强弱,氯气通入溴化钠溶液中,氯气氧化溴离子为溴单质,溶液呈橙红色;若利用装置A、E进行乙烯与溴水反应的实验,乙烯制备需要控制反应温度170°C,实验装置中需要用温度计控制反应液的温度;
(5)将装置B、C分别与F相连后,进行H2S与SO2反应的实验,B是制备硫化氢气体的发生装置,C是二氧化硫气体制备的装置,通入F中二氧化硫氧化硫化氢生成硫单质,容器中压强减小,会产生倒吸,同时F烧杯可以吸收剩余气体二氧化硫或硫化氢有毒气体.
解答 解:Ⅰ、(1)实验中干燥氨气可以用碱石灰或生石灰,故选ad;
(2)依据制备氯气装置是利用二氧化锰和浓盐酸加热反应,生成的氯气中含有氯化氢和水蒸气,通过饱和食盐水除去氯化氢,通过浓硫酸除去水蒸气;
故答案为:饱和食盐水、浓硫酸;
(3)实验时打开开关1、3,关闭2向烧瓶中通入氯气,然后关闭1、3,打开2,向烧瓶中缓慢通入一定量的氨气,实验一段时间后烧瓶内出现浓厚的白烟并在容器内壁凝结,已知氯气与氨气可发生反应:3Cl2+2NH3→N2+6HCl,依据反应化学方程式判断是生成的氯化氢和过量氨气反应生成的氯化铵;铵根离子的检验方法是,取少量固体于试管中,加入适量NaOH溶液并加热,在管口用湿润的红色石蕊试纸检验产生的气体,若湿润的红色石蕊试纸变蓝,证明固体中有NH4+;
故答案为:氯气;取少量固体于试管中,加入适量NaOH溶液并加热,在管口用湿润的红色石蕊试纸检验产生的气体,若湿润的红色石蕊试纸变蓝,证明固体中有NH4+;
(4)利用装置A、E,可设计实验比较Cl-和Br-的还原性强弱,氯气通入溴化钠溶液中,氯气氧化溴离子为溴单质,反应为:Cl2+2NaBr=Br2+2NaCl,溴单质溶于水溶液呈橙红色;若利用装置A、E进行乙烯与溴水反应的实验,装置A是乙烯制备装置,需要控制反应温度170°C,实验装置中需要用温度计控制反应液的温度,所以要将分液漏斗改为温度计,并使温度计水银球没入烧瓶内液面下;
故答案为:装置E中的NaBr溶液变橙红色;将分液漏斗改为温度计,并使温度计水银球没入烧瓶内液面下;
(5)将装置B、C分别与F相连后,进行H2S与SO2反应的实验,B是制备硫化氢气体的发生装置,C是二氧化硫气体制备的装置,通入F中二氧化硫氧化硫化氢生成硫单质,容器中压强减小,会产生倒吸,同时F烧杯可以吸收剩余气体二氧化硫或硫化氢有毒气体;
故答案为:证明烧瓶中压强减少,同时吸收剩余气体二氧化硫或硫化氢有毒气体.
点评 本题考查物质性质的实验验证和实验设计方法,反应现象的分析判断,装置选择,掌握实验基础和物质性质是解题关键,题目难度中等.

| A. | HF溶液保存在玻璃试剂瓶中 | |
| B. | 液溴应保存在棕色磨口玻璃塞的试剂瓶中,并加少量水进行水封 | |
| C. | 为防止被氧化,FeSO4溶液存放在加有少量铁粉的试剂瓶中 | |
| D. | 硝酸应装在棕色瓶中密封避光保存 |
| A. | Zn+H2SO4═ZnSO4+H2↑ | B. | 2KClO3$\frac{\underline{\;MnO_{2}\;}}{△}$2KCl+3O2↑ | ||
| C. | S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2 | D. | H2+Cl2$\frac{\underline{\;点燃\;}}{\;}$2HCl |
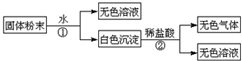
以制革工业产生的污泥为原料,回收污泥中三价铬的工艺流程如图所示,(硫酸浸取液中金属离子主要是Cr3+,其次是Fe3+、Al3+、Cu2+、Mg2+):
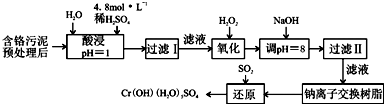
部分阳离子常温下以氢氧化物形式沉淀时溶液的pH见下表:
| 阳离子 | Fe3+ | Fe2+ | Mg2+ | Al3+ | Cu2+ | Cr3+ |
| 开始沉淀时的pH | 1.9 | 7.0 | -- | -- | 4.7 | -- |
| 沉淀完全时的pH | 3.2 | 9.0 | 11.1 | 8 | 6.7 | 9 (>9溶解) |
A.将含铬污泥粉碎并适当延长浸取时间 B.升高温度不断搅拌 C.多次浸取,合并浸取液 D.缩短浸取时间
(2)氧化过程中加入H2O2,除了能把Cr3+氧化为Cr2O72-外,另一个作用是2Fe2++2H++H2O2=2Fe3++2H2O(用离子方程式表示)
(3)过滤Ⅱ产生的沉淀是Fe(OH)3、Al(OH)3、Cu(OH)2,(填化学式)
(4)钠离子交换树脂的原理为:Mn++nNaR→MRn+nNa+,被交换的杂质离子是Ca2+,Mg2+(填离子符号)
(5)每生成1molCr(OH)(H2O)3SO4,消耗SO2的物质的量为1.5mol
(6)工业上可用电解法处理含Cr2O72-的酸性废水,具体方法是将含Cr2O72-的酸性废水放入电解槽内,加入适量的NaCl,以铁和石墨为电极进行电解,经过一段时间后,生成Cr(OH)3和Fe(OH)3沉淀除去
①铁电极与直流电源的正极(填“正极”或“负极”)相连,加入适量NaCl的目的是增大溶液导电能力
②若电解后的溶液中c(Fe3+)为2.0×10-13mol•L-1,则溶液中为3.0×10-6mol/L(已知Ksp[Fe(OH)3]=4.0×10-38,Ksp[Fe(OH)3]=6.0×10-31)
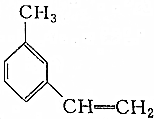 的命名正确的是( )
的命名正确的是( )| A. | 1-甲基-3-乙基苯 | B. | 1-甲基-3-苯乙烯 | C. | 间甲基苯乙烯 | D. | 间乙基甲苯 |
 ;
;

 ②
②
 (请用化学方程式表达).
(请用化学方程式表达). 等(任写一种).
等(任写一种).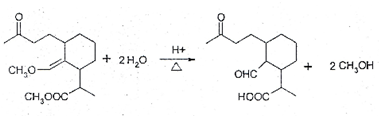 .
.