题目内容
8.下列关于有机物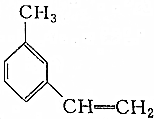 的命名正确的是( )
的命名正确的是( )| A. | 1-甲基-3-乙基苯 | B. | 1-甲基-3-苯乙烯 | C. | 间甲基苯乙烯 | D. | 间乙基甲苯 |
分析 该有机物的主链为苯乙烯,编号从乙烯连接的苯环碳原子开始,甲基处于3号C,其名称为3-甲基苯乙烯,或间甲基苯乙烯,据此进行解答.
解答 解: 中主链为苯乙烯,编号从乙烯基连接的苯环碳原子开始,甲基在3号C,所以该有机物名称为:3-甲基苯乙烯,
中主链为苯乙烯,编号从乙烯基连接的苯环碳原子开始,甲基在3号C,所以该有机物名称为:3-甲基苯乙烯,
按照习惯命名法,甲基和乙烯基处于间位,该有机物还可以命名为:间甲基苯乙烯,
故选C.
点评 本题考查了有机物命名,题目难度不大,正确选取该有机物主链为解答关键,注意熟练掌握常见有机物的命名原则,试题培养了学生的分析能力及灵活应用能力.

练习册系列答案
相关题目
18.设NA为阿伏伽德罗常数的数值,下列说法不正确的是( )
| A. | 两份均为18g的Al片分别与足量的盐酸和NaOH溶液充分转移电子总数均为2NA | |
| B. | 1 molCu和2 mol热浓硫酸充分反应,可生成NA个SO2分子 | |
| C. | 标准状况下,14g N2和C2H4混合气体的体积为11.2L | |
| D. | 3mol单质Fe完全转变为Fe3O4,失去8NA个电子 |
16.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | PH=1的稀硫酸中含有的H+数为0.1NA | |
| B. | 1mol苯分子中含有的碳碳双键数为3NA | |
| C. | 18gH2O中含有的质子数为10NA | |
| D. | 50mL12mol•L-1的盐酸与足量的MnO2共热,生成的Cl2分子数为0.15NA |
3.某实验小组用工业上废渣(主要成分Cu2S和Fe2O3)制取纯铜和绿矾(FeSO4•7H2O)产品,设计流程如图1:
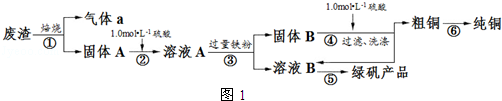
(1)在实验室中,欲用98%的浓硫酸(密度为1.84g•mL-1)配制500mL1.0mol•L-1的硫酸,需要的仪器除量筒、烧杯、玻璃棒外、胶头滴管,还有500mL容量瓶.
(2)该小组同学设计如图2装置模拟废渣在过量氧气中焙烧,并验证废渣中含硫元素.
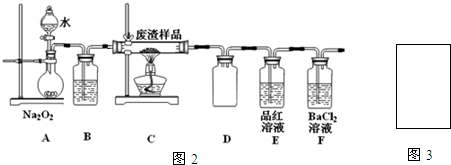
①装置A中反应的化学方程式为2Na2O2+2H2O=4NaOH+O2↑;D装置作用安全瓶,E装置中的现象是品红溶液红色褪去
②当F装置中出现白色沉淀时,反应离子方程式为2SO2+O2+2H2O+2Ba2+=2BaSO4↓+4H+
③反应装置不完善,为避免空气污染,在图3方框中补全装置图,并注明试剂名称.
(3)从图4选择合适的装置,写出步骤⑤中进行的操作顺序cb(填序号)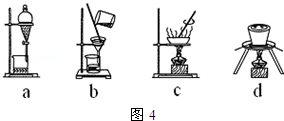
(4)步骤⑥中由粗铜得到纯铜的方法为电解精炼(填写名称).
(5)为测定产品中绿矾的质量分数,称取30.0g样品溶于水配成250mL溶液,取25.00mL溶液于锥形瓶中,用0.1000mol•L-1酸性KMnO4溶液进行滴定,反应为:10FeSO4+8H2SO4+2KMnO4═2MnSO4+5Fe2(SO4)3+K2SO4+8H2O.实验所得数据如表所示:
①第1组实验数据出现异常,造成这种异常的原因可能是c(填代号).
a.酸式滴定管用蒸馏水洗净后未用标准液润洗
b.锥形瓶洗净后未干燥
c.滴定终点时俯视读数
d.滴定前尖嘴有气泡,滴定后气泡消失
②根据表中数据,计算所得产品中绿矾的质量分数为92.7%.

(1)在实验室中,欲用98%的浓硫酸(密度为1.84g•mL-1)配制500mL1.0mol•L-1的硫酸,需要的仪器除量筒、烧杯、玻璃棒外、胶头滴管,还有500mL容量瓶.
(2)该小组同学设计如图2装置模拟废渣在过量氧气中焙烧,并验证废渣中含硫元素.

①装置A中反应的化学方程式为2Na2O2+2H2O=4NaOH+O2↑;D装置作用安全瓶,E装置中的现象是品红溶液红色褪去
②当F装置中出现白色沉淀时,反应离子方程式为2SO2+O2+2H2O+2Ba2+=2BaSO4↓+4H+
③反应装置不完善,为避免空气污染,在图3方框中补全装置图,并注明试剂名称.
(3)从图4选择合适的装置,写出步骤⑤中进行的操作顺序cb(填序号)

(4)步骤⑥中由粗铜得到纯铜的方法为电解精炼(填写名称).
(5)为测定产品中绿矾的质量分数,称取30.0g样品溶于水配成250mL溶液,取25.00mL溶液于锥形瓶中,用0.1000mol•L-1酸性KMnO4溶液进行滴定,反应为:10FeSO4+8H2SO4+2KMnO4═2MnSO4+5Fe2(SO4)3+K2SO4+8H2O.实验所得数据如表所示:
| 滴定次数 | 1 | 2 | 3 | 4 |
| KMnO4溶液体积/mL | 19.10 | 20.02 | 19.98 | 20.00 |
a.酸式滴定管用蒸馏水洗净后未用标准液润洗
b.锥形瓶洗净后未干燥
c.滴定终点时俯视读数
d.滴定前尖嘴有气泡,滴定后气泡消失
②根据表中数据,计算所得产品中绿矾的质量分数为92.7%.
13.下列反应可以在烃分子中引入卤素原子的是( )
| A. | 苯和溴水共热 | B. | 光照甲苯与氯气的混合物 | ||
| C. | 溴乙烷与NaOH溶液共热 | D. | 乙烷通入溴的四氯化碳溶液中 |
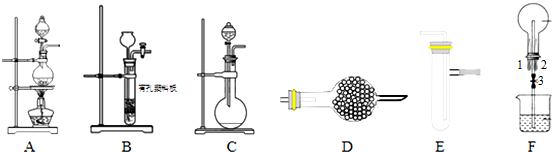
20.下列实验操作或装置不符合实验要求的是( )
| 选项 | A | B | C | D |
| 操作 | 从CCl4萃取溴水中溴后的混合液中分离 | 二氧化锰与浓盐酸反应制干燥氯气 | 可用于制备并观察氢氧化铁沉淀 | 检查装置气密性 |
| 实验装置 | 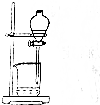 | 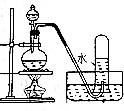 | 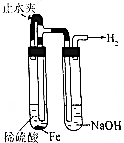 | 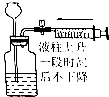 |
| A. | A | B. | B | C. | C | D. | D |
14.已知:C(金刚石,固)→C(石墨,固)+1.9kJ,则下列判断正确的是( )
| A. | 石墨比金刚石稳定 | |
| B. | 等质量的石墨比金刚石能量高 | |
| C. | 发生了物理变化 | |
| D. | 金刚石转化为石墨没有化学键的断裂与生成 |
15.化学是21世纪最富有创造性的中心学科•下列有关说法不正确的是( )
| A. | 按照规定对生活废弃物进行分类放置,实现资源再利用 | |
| B. | 防治环境污染、开发智能软件、合成新材料等,都属于化学研究的领域 | |
| C. | 利用人工光合成反应,将二氧化碳转化为碳氢化合物作燃料,属于低碳技术 | |
| D. | 液晶态介于晶体状态和液态之间,液晶具有有一定程度的晶体的有序性和液体的流动性 |