题目内容
19.NA为阿伏加德罗常数,下列叙述错误的是( )| A. | 18gNH4+中含有的电子数为11NA | |
| B. | 12g石墨中含有的共价键数为1.5NA | |
| C. | 标准状况下,22.4LNO2和CO2混合物中含有原子总数为3NA | |
| D. | 1 mol Na与足量O2反应,生成 Na2O和Na2O2的混合物,钠失去NA个电子 |
分析 A、求出铵根离子的物质的量,然后根据铵根离子中含10个电子来分析;
B、石墨中每个碳原子与气体3个C形成3个共价键,利用均摊法计算出1molC含有的共价键;
C、求出混合气体的物质的量,然后根据NO2中存在平衡:2NO2?N2O4来分析;
D、钠和氧气反应后变为-1价.
解答 解:A、18g铵根离子的物质的量为1mol,而铵根离子中含10个电子,故1mol铵根离子中含10NA个电子,故A错误;
B、12g石墨中含有1molC,1mol碳原子与其它3mol碳原子形成了3mol共价键,1mol碳原子形成的共价键为:$\frac{1}{2}$×3mol=1.5mol,含有的共价键数为1.5NA,故B正确;
C、标况下22.4LNO2和CO2的物质的量为1mol,而NO2中存在平衡:2NO2?N2O4,故1mol混合物中不止是NO2和CO2,还有N2O4,故含有的原子个数多于3NA个,故C错误;
D、钠和氧气反应后变为-1价,故1mol钠反应后失去NA个电子,故D正确.
故选AC.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
9.下列说法中正确的是( )
| A. | 1mol CO2和1mol CO所占的体积相同,所含分子数相同 | |
| B. | 1g CO和1g CO2所占的体积不同,所含分子数不同 | |
| C. | 在任何情况下,1mol CO2和64g SO2所含有分子数和原子总数都相同 | |
| D. | 某物质若含阿伏加德罗常数个微粒,该物质在标准状况下体积约为22.4L |
10.下列化学用语对应正确的是( )
| A. | HClO的结构式:H-Cl-O | B. | C(CH3)3(OH)的名称:1,1-二甲基乙醇 | ||
| C. | Na2O2的电子式: | D. | Mg2+的电子排布式:1S22S22P6 |
11.下列关于氯水的叙述中正确的是( )
| A. | 新制氯水中只含有Cl2和H2O两种物质 | |
| B. | 新制氯水可以使蓝色石蕊试纸先变红后褪色 | |
| C. | 光照氯水有气泡逸出,逸出的气体只有氯气 | |
| D. | 氯水放置数天后酸性减弱 |
7.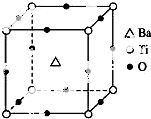 如图所示晶体结构是一种具有优良的压电功能的铁片晶体材料的最小结构单元(晶胞),晶体内与每个“Ti”紧邻的氧原子数和这种晶体材料的化学式分别是( )
如图所示晶体结构是一种具有优良的压电功能的铁片晶体材料的最小结构单元(晶胞),晶体内与每个“Ti”紧邻的氧原子数和这种晶体材料的化学式分别是( )
 如图所示晶体结构是一种具有优良的压电功能的铁片晶体材料的最小结构单元(晶胞),晶体内与每个“Ti”紧邻的氧原子数和这种晶体材料的化学式分别是( )
如图所示晶体结构是一种具有优良的压电功能的铁片晶体材料的最小结构单元(晶胞),晶体内与每个“Ti”紧邻的氧原子数和这种晶体材料的化学式分别是( )| A. | 8 BaTi8O12 | B. | 8 BaTi4O9 | C. | 6 BaTiO3 | D. | 3 BaTi2O3 |
 ,从共用电子对是否偏移的角度,说明在H2O2中的共价键的不同之处:H、O之间极性共价键,O、O之间非极性共价键.
,从共用电子对是否偏移的角度,说明在H2O2中的共价键的不同之处:H、O之间极性共价键,O、O之间非极性共价键. ,
, ,
, ,
,