题目内容
能正确表示下列反应的离子方程式为( )
| A、硫化亚铁溶于稀硝酸中:FeS+2H+═Fe2++H2S↑ |
| B、少量CO2通入硅酸钠溶液中:SiO32-+2CO2+2H2O═H2SiO3↓+2HCO3- |
| C、含等物质的量的KHCO3和Ba(OH)2溶液混合:HCO3-+Ba2++OH-═BaCO3↓+H2O |
| D、硫化钠水溶液呈碱性:S2-+2H2O?H2S+2OH- |
考点:离子方程式的书写
专题:离子反应专题
分析:A.硝酸具有氧化性,能氧化FeS,因此产物应该是硝酸铁、硫酸和一氧化氮;
B.碳酸氢根离子酸性大于硅酸,硅酸钠溶液与二氧化碳反应生成硅酸和碳酸钠;
C.等物质的量碳酸氢钾与氢氧化钡反应生成碳酸钡、水、KOH;
D.硫化钠水溶液呈碱性是因硫离子水解造成的,且水解分步进行,以第一步为主.
B.碳酸氢根离子酸性大于硅酸,硅酸钠溶液与二氧化碳反应生成硅酸和碳酸钠;
C.等物质的量碳酸氢钾与氢氧化钡反应生成碳酸钡、水、KOH;
D.硫化钠水溶液呈碱性是因硫离子水解造成的,且水解分步进行,以第一步为主.
解答:
解:A.硫化亚铁溶于稀硝酸中,亚铁离子被硝酸氧化成铁离子,正确的离子方程式为:FeS+4H++NO3-=Fe3++S↓+NO↑+2H2O,故A错误;
B.向硅酸钠溶液中通入少量二氧化碳,反应生成碳酸钠,正确的离子方程为:SiO32-+CO2+2H2O═H4SiO4↓+CO32-,故B错误;
C.含等物质的量的KHCO3和Ba(OH)2溶液混合,氢氧根离子过量,离子方程式按照碳酸氢钾的组成书写,反应的离子方程式为:HCO3-+Ba2++OH-═BaCO3↓+H2O,故C正确;
D.硫化钠水溶液中,硫离子水解溶液呈碱性,硫离子的水解分步进行,水解方程式写出第一步即可,正确的离子方程式为:S2-+H2O?HS-+OH-,故D错误;
故选C.
B.向硅酸钠溶液中通入少量二氧化碳,反应生成碳酸钠,正确的离子方程为:SiO32-+CO2+2H2O═H4SiO4↓+CO32-,故B错误;
C.含等物质的量的KHCO3和Ba(OH)2溶液混合,氢氧根离子过量,离子方程式按照碳酸氢钾的组成书写,反应的离子方程式为:HCO3-+Ba2++OH-═BaCO3↓+H2O,故C正确;
D.硫化钠水溶液中,硫离子水解溶液呈碱性,硫离子的水解分步进行,水解方程式写出第一步即可,正确的离子方程式为:S2-+H2O?HS-+OH-,故D错误;
故选C.
点评:本题考查离子反应方程式的书写,题目难度中等,明确发生的化学反应是解答本题的关键,并注意离子反应方程式的书写方法,试题有利于培养学生灵活应用所学知识的能力.

练习册系列答案
 出彩同步大试卷系列答案
出彩同步大试卷系列答案
相关题目
下列对0.1mol/L的醋酸溶液和0.1mol/L的醋酸钠溶液说法不正确的是( )
| A、向两种溶液中加入少量固体醋酸钠,电离平衡和水解平衡都逆向移动 |
| B、两种溶液中CH3COO-浓度不同 |
| C、将等体积的两种溶液混合,若c(Na+)<c(CH3COO-),则c(CH3COOH)<c(CH3COO-) |
| D、将两种溶液混合,醋酸的电离平衡和醋酸钠的水解平衡都被抑制 |
下列各项中表达正确的是( )
A、F原子结构示意图: |
B、次氯酸电子式: |
| C、H、D、T表示同一种核素 |
D、CH4分子的球棍模型: |
物质的量相等的Na2CO3和 NaHCO3分别与足量的盐酸反应,得到CO2的物质的量之比为( )
| A、1:1 | B、2:1 |
| C、1:2 | D、1:3 |
下列离子方程式正确的是( )
| A、铁和盐酸反应:2Fe+6H+=2Fe3++3H2↑ |
| B、氯化铁和铜反应:Fe3++Cu=Fe2++Cu2+ |
| C、石灰水与碳酸钠溶液混合:Ca2++CO32-=CaCO3↓ |
| D、硫酸氢钠溶液中加入氢氧化钡溶液至中性:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O |
1L(标准状况下)某烃,完全燃烧生成CO2和水蒸气在273℃,1.01×105 Pa下,混合气体体积为y L,当冷却至标准状况时气体体积为x L,下列用x、y表示该烃的化学式正确的是( )
| A、CxHy |
| B、CxHy -x |
| C、CxH2y-2x |
| D、CxHy-2x |
以石化产品乙烯、丙烯为原料合成厌氧胶的流程如图.关于该过程的相关叙述不正确的是( )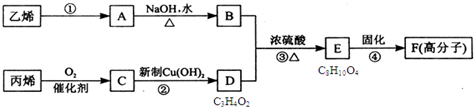

| A、反应④的反应类型是加聚 |
| B、物质A是卤代烃 |
| C、物质B催化氧化后可以得到乙醛 |
| D、1mol物质E最多可以消耗2molNaOH |
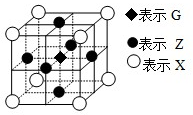 已知:E、G、Q、R、T、X、Y、Z都是周期表中前四周期的元素,它们的核电荷数依次增大.E的简单阴离子最外层有2个电子,G原子最外层电子数是内层电子数的两倍,X元素最外层电子数与最内层电子数相同.T2R的晶体类型是离子晶体,Y原子基态3p原子轨道上有2个未成对电子,其单质晶体类型属于原子晶体;在元素周期表中Z元素位于第10列.
已知:E、G、Q、R、T、X、Y、Z都是周期表中前四周期的元素,它们的核电荷数依次增大.E的简单阴离子最外层有2个电子,G原子最外层电子数是内层电子数的两倍,X元素最外层电子数与最内层电子数相同.T2R的晶体类型是离子晶体,Y原子基态3p原子轨道上有2个未成对电子,其单质晶体类型属于原子晶体;在元素周期表中Z元素位于第10列.