题目内容
物质的量相等的Na2CO3和 NaHCO3分别与足量的盐酸反应,得到CO2的物质的量之比为( )
| A、1:1 | B、2:1 |
| C、1:2 | D、1:3 |
考点:化学方程式的有关计算
专题:计算题
分析:设Na2CO3和NaHCO3的物质的量分别为1mol,根据方程式得关系式Na2CO3~CO2,NaHCO3~CO2,产生的CO2的物质的量分别为1mol,即放出CO2的物质的量1:1.
解答:
解:设Na2CO3和NaHCO3的物质的量分别为1mol,Na2CO3和 NaHCO3分别与足量的盐酸反应Na2CO3+2HCl=2NaCl+CO2↑+H2O,NaHCO3+HCl=NaCl+CO2↑+H2O 根据方程式得关系式Na2CO3~CO2,NaHCO3~CO2,都为1mol的Na2CO3和 NaHCO3分别与足量的盐酸反应,产生的CO2的物质的量分别为1mol,即放出CO2的物质的量1:1,
故选A.
故选A.
点评:本题考查碳酸钠与碳酸氢钠的性质,明确发生的化学反应是解答本题的关键,题目较简单.

练习册系列答案
 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案
相关题目
下列叙述正确的是( )
| A、Na2O是淡黄色固体,和水反应生成NaOH,是碱性氧化物 |
| B、在Na2O2与水的反应中,氧化剂是Na2O2,还原剂是水 |
| C、SO2通入品红中红色褪去,加热后红色恢复 |
| D、将Cl2与SO2按物质的量之比1:1通入紫色石蕊试液,溶液先变红后褪色 |
下列说法不正确的是( )
| A、纳米材料是指一种称为“纳米”的新物质制成的材料 |
| B、复合材料一般有强度高、质量轻、耐高温、耐腐蚀等优异性能,其综合性质超过了单 一材料 |
| C、光导纤维是以二氧化硅为主要原料制成的 |
| D、合成纤维的主要原料是石油、天然气、煤等 |
下列物质的分类结果全部正确的是( )
| A、CO--酸性氧化物 Na2O2--碱性氧化物 Al2O3--两性氧化物 |
| B、漂白粉--混合物 胆矾--纯净物 HD--单质 |
| C、纯碱--碱 硫化氢--酸 小苏打--酸式盐 |
| D、盐酸--强电解质 硫酸钡--强电解质 醋酸--弱电解质 |
下列说法正确的是( )
| A、可逆反应在其他条件不变时,升高温度,可以减小反应的活化能,加快反应速率 |
| B、S电子云是球形对称的,P电子云是纺锤形,电子云中每个小黑点代表一个电子 |
| C、氮原子的第一电离能低于氧原子的第一电离能,因为氮比氧非金属性弱 |
| D、Fe3+ 比Fe2+稳定,因为Fe3+价电子构型是3d5,d亚层处于半充满状态,稳定 |
能正确表示下列反应的离子方程式为( )
| A、硫化亚铁溶于稀硝酸中:FeS+2H+═Fe2++H2S↑ |
| B、少量CO2通入硅酸钠溶液中:SiO32-+2CO2+2H2O═H2SiO3↓+2HCO3- |
| C、含等物质的量的KHCO3和Ba(OH)2溶液混合:HCO3-+Ba2++OH-═BaCO3↓+H2O |
| D、硫化钠水溶液呈碱性:S2-+2H2O?H2S+2OH- |
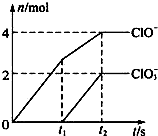 向一定量的石灰乳中通入一定量的氯气,二者恰好完全反应(发生的反应均为放热反应).生成物中有三种含氯元素的离子,其中两种离子的物质的量(n)与反应时间(t)的曲线如图所示.已知,生成ClO3-的反应为:6Ca(OH)2+6Cl2
向一定量的石灰乳中通入一定量的氯气,二者恰好完全反应(发生的反应均为放热反应).生成物中有三种含氯元素的离子,其中两种离子的物质的量(n)与反应时间(t)的曲线如图所示.已知,生成ClO3-的反应为:6Ca(OH)2+6Cl2