题目内容
6.1999年是人造元素丰收年,一年间得到第114、117和118号三个新元素.按已知的原子结构规律,117号元素应是第七周期第ⅦA族元素,它的单质在常温常压下最可能呈现的状态是固(气、液、固选一填入)体.分析 第七周期稀有气体的原子序数为118,可知117号元素处于第七周期ⅦA族,卤族元素从上到下单质的状态由气体→液体→固体递变,以此来解答.
解答 解:第七周期稀有气体的原子序数为118,可知117号元素处于第七周期ⅦA族,由同族元素单质的性质变化规律可知,117号浩元素的单质在常温常压下最可能呈现的状态是固体,故答案为:七;ⅦA;固.
点评 本题考查元素周期表的结构及应用,为高频考点,把握稀有气体元素的位置推断其它元素的位置为解答的关键,注意元素周期律的应用,题目难度不大.

练习册系列答案
 步步高达标卷系列答案
步步高达标卷系列答案
相关题目
17.在实验室进行物质制备,下列从原料及试剂分别制取相应的最终产物的设计中,理论上正确、操作上可行、经济上合理的是( )
| A. | C$\stackrel{在空气中燃烧}{→}$ CO$\stackrel{CuO△}{→}$ CO2$\stackrel{NaOH溶液}{→}$ Na2CO3 | |
| B. | Cu$\stackrel{AgNO_{3}溶液}{→}$ Cu(NO3)2溶液$\stackrel{NaOH溶液}{→}$ Cu(OH)2 | |
| C. | Fe $\stackrel{点燃}{→}$ Fe2O3$\stackrel{H_{2}SO_{4}溶液}{→}$ Fe2(SO4)3溶液 | |
| D. | CaO$\stackrel{H_{2}O}{→}$ Ca(OH)2溶液$\stackrel{Na_{2}CO_{3}溶液}{→}$ NaOH溶液 |
14.为确定某溶液的离子组成,分别进行如下实验:
①测定溶液的pH,溶液显强碱性.
②取少量溶液加入稀盐酸至溶液呈酸性,产生无刺激性、能使澄清石灰水变浑浊的气体.
③在上述溶液中再滴加Ba(NO3)2溶液,产生白色沉淀.
④取上层清液继续滴加Ba(NO3)2溶液至无沉淀时,再滴加AgNO3溶液,产生白色沉淀.
根据实验以下推测正确的是( )
①测定溶液的pH,溶液显强碱性.
②取少量溶液加入稀盐酸至溶液呈酸性,产生无刺激性、能使澄清石灰水变浑浊的气体.
③在上述溶液中再滴加Ba(NO3)2溶液,产生白色沉淀.
④取上层清液继续滴加Ba(NO3)2溶液至无沉淀时,再滴加AgNO3溶液,产生白色沉淀.
根据实验以下推测正确的是( )
| A. | 不能确定HCO3-离子是否存在 | B. | 可能有CO32-离子 | ||
| C. | 一定有Cl-离子存在 | D. | 一定有SO42-离子 |
11.分别往含有下列离子的溶液中通入氯气,离子浓度不会减少的是( )
| A. | Ag+ | B. | HCO3- | C. | I- | D. | Na+ |
18.处于平衡状态的反应2H2S(g)?2H2(g)+S2(g)△H>0,不改变其他条件的情况下,不合理的说法是( )
| A. | 加入催化剂,反应途径将发生改变,但△H不会改变 | |
| B. | 升高温度,正逆反应速率都增大,H2S分解率也增大 | |
| C. | 增大压强,平衡向逆反应方向移动,将引起体系温度升高 | |
| D. | 若体系恒容,注入一些H2后平衡逆向移动,达到新平衡,H2浓度比原平衡小 |
15.J、L、M、R、T是原子序数依次增大的短周期主族元素,J、R在周期表中的相对位置如下表;J元素最低负化合价的绝对值与其原子最外层电子数相等;M是地壳中含量最多的金属元素.
(1)元素T的最高价含氧酸具有强酸性;T在周期表中的位置是第三周期第ⅦA族.
(2)化合物甲的分子由两个J原子和两个氢原子构成,甲的电子式是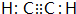 .
.
(3)一定条件下,R元素的最高价氧化物乙在固定容积的密闭容器中发生分解反应(△H>0),达到平衡后,仅改变下表中反应条件x,该平衡体系中随x递增,y递减的是ac(选填序号)
(4)L的最简单气态氢化物丙的水溶液显碱性,在微电子工业中,丙的水溶液可作H2O2的清除剂,反应的产物不污染环境,其化学方程式为NH3+3H2O2=N2+6H2O.
(5)在298K下,J、M的单质各1mol完全燃烧,分别放出热量以akJ和bkJ时.又知一定条件下,M的单质能将J从它的最高价氧化物中置换出来,写出此置换反应的热化学方程式:4Al(s)+3CO2(g)=3C(s)+2Al2O3(s)△H=(+3a-4b)kJ/mol.(注:题中所设单质均为最稳定单质)
(6)用M单质作阳极,J单质作阴极,Ca(HCO3)2溶液作电解液,进行电解,阴极生成的气体和沉淀分别是H2、CaCO3,阳极也生成气体和沉淀,写出阳极的电极反应式Al-3e-+3HCO3-=Al(OH)3+3CO2↑.
| J | ||||
| R |
(2)化合物甲的分子由两个J原子和两个氢原子构成,甲的电子式是
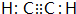 .
.(3)一定条件下,R元素的最高价氧化物乙在固定容积的密闭容器中发生分解反应(△H>0),达到平衡后,仅改变下表中反应条件x,该平衡体系中随x递增,y递减的是ac(选填序号)
| 选项 | a | b | c | d |
| x | 温度 | 温度 | 加入氧气 | 加入乙的物质 |
| y | 乙的物质的量 | 平衡常数K | 乙的转化率 | 生成物物质的量总和 |
(5)在298K下,J、M的单质各1mol完全燃烧,分别放出热量以akJ和bkJ时.又知一定条件下,M的单质能将J从它的最高价氧化物中置换出来,写出此置换反应的热化学方程式:4Al(s)+3CO2(g)=3C(s)+2Al2O3(s)△H=(+3a-4b)kJ/mol.(注:题中所设单质均为最稳定单质)
(6)用M单质作阳极,J单质作阴极,Ca(HCO3)2溶液作电解液,进行电解,阴极生成的气体和沉淀分别是H2、CaCO3,阳极也生成气体和沉淀,写出阳极的电极反应式Al-3e-+3HCO3-=Al(OH)3+3CO2↑.