题目内容
1.已知反应3O2(g)=2O3(g)的△H<0、△S<0,对此反应叙述正确的是( )| A. | 该反应在任何情况下均能自发进行 | |
| B. | 该反应在任何情况下均不能自发进行 | |
| C. | 该反应在一定条件下能自发进行 | |
| D. | 条件不足,无法判断 |
分析 化学反应能否自发进行,取决于焓变和熵变的综合判据,当△G=△H-T•△S<0时,反应能自发进行.
解答 解:化学反应能否自发进行,取决于焓变和熵变的综合判据,当△G=△H-T•△S<0时,反应能自发进行,
已知3O2(g)=2O3(g)的△H<0、△S<0,所以低温下反应可能自发进行△G=△H-T•△S<0,该反应在一定条件下能自发进行,
故选C.
点评 本题考查反应热与焓变,题目难度不大,注意自由能判据的应用.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
12.向NaOH溶液中缓慢通入CO2气体,溶液中CO32-的物质的量与通入CO2物质的量的关系图如下.下列关于图中a、b两点溶液的说法错误的是( )


| A. | a、b两点溶液中水的电离程度相同 | |
| B. | a、b两点溶液的pH满足:pH(a)>pH(b) | |
| C. | c点溶液满足:c(Na+)>c(CO3 2-)>c(OH-)>c(HCO3-)>c(H+) | |
| D. | a、b、c三点溶液都满足:c(Na+)+c(H+)=c(HCO3-)+2c(CO3 2-)+c(OH-) |
9.某溶液中含H+、SO42-、NO3-三种离子,其中H+、SO42-的物质的量浓度分别为7.0mol•L-1和2.0mol•L-1.取该溶液20mL,加入3.2g铜粉,加热使它们充分反应,产生的气体在标准状况下的体积约为( )
| A. | 0.75 L | B. | 0.336 L | C. | 1.5 L | D. | 0.448 L |
16.下列有关实验操作正确的是( )
| A. | 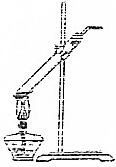 加热NaHCO3固体 | B. |  中和滴定 | ||
| C. |  用苯萃取碘水分离苯层的操作 | D. | 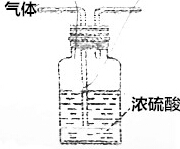 除去氨气中的水蒸气 |
6.手机中使用的锂(Li)电池电板是新型的高能电池,以质量轻、电容量大而受到普遍重视,目前已制成多种功能的锂电池,某种锂电池的总反应可表示为Li+MnO2=LiMnO2,在此反应中锂元素的化合价变化0→+1,下列对锰元素的化合价变化判断正确的是( )
| A. | +4→+3 | B. | +2→+3 | C. | 0→+2 | D. | -4→-2 |
13.甲烷和乙烷混合气体完全燃烧时,消耗相同状况下氧气的体积是混合气体的2.8倍,则甲烷与乙烷的体积比是( )
| A. | 8:7 | B. | 5:7 | C. | 7:8 | D. | 7:5 |
10.室温下,0.1mol•L-1NaHCO3溶液的pH=8.31,有关该溶液的判断正确的是( )
| A. | c(Na+)>c(OH-)>c(HCO3-)>c(CO32-)>c(H+) | |
| B. | Ka1(H2CO3)•Ka2(H2CO3)<KW | |
| C. | c(H+)+c(Na+)=c(OH-)+c(HCO3-)+c(CO32-) | |
| D. | 加入适量NaOH溶液后:c(Na+)=c(H2CO3)+c(HCO3-)+c(CO32-) |
20.下列五种物质中:①水 ②乙醇 ③醋酸 ④苯酚 ⑤碳酸.羟基氢原子的活性从大到小顺序是( )
| A. | ③⑤④①② | B. | ③④②①⑤ | C. | ④①②⑤③ | D. | ③②④①⑤ |