题目内容
 水系锂电池具有安全、环保和价格低廉等优点成为当前电池研究领域的热点.以钒酸钠(NaV3O8)为正极材料的电极反应式为:NaV3O8+xLi++xe-=NaLixV3O8,则下列说法不正确的是( )
水系锂电池具有安全、环保和价格低廉等优点成为当前电池研究领域的热点.以钒酸钠(NaV3O8)为正极材料的电极反应式为:NaV3O8+xLi++xe-=NaLixV3O8,则下列说法不正确的是( )| A、放电时,负极的电极反应式:Li-e-═Li+ |
| B、充电过程中Li+从阳极向阴极迁移 |
| C、充电过程中阳极的电极反应式为NaLixV3O8-xe-=NaV3O8+xLi+,NaLixV3O8中钒的化合价发生变化 |
| D、该电池可以用硫酸钠溶液作电解质 |
考点:化学电源新型电池
专题:
分析:放电时,b电极Li作负极,电极反应式为Li-e-═Li+,a作正极,电极反应式为NaV3O8+xLi++xe-=NaLixV3O8,则电池反应式为NaV3O8+xLi=NaLixV3O8,充电时,阴极、阳极电极反应式与负极、正极反应式正好相反,充电时,阳离子向阴极移动、阴离子向阳极移动,据此分析解答.
解答:
解:放电时,b电极Li作负极,Li失电子发生氧化反应,电极反应式为Li-e-═Li+,故A正确;
B.充电时,阳离子向阴极移动、阴离子向阳极移动,所以Li+从阳极向阴极迁移,故B正确;
C.充电时,阴极、阳极电极反应式与负极、正极反应式正好相反,所以阳极的电极反应式为NaLixV3O8-xe-=NaV3O8+xLi+,NaLixV3O8中Na、O、Li元素化合价不变,则钒的化合价发生变化,失电子发生氧化反应,故C正确;
D.Li极易和水反应生成LiOH和氢气,所以电池中不可以用硫酸钠溶液作电解质溶液,故D错误;
故选D.
B.充电时,阳离子向阴极移动、阴离子向阳极移动,所以Li+从阳极向阴极迁移,故B正确;
C.充电时,阴极、阳极电极反应式与负极、正极反应式正好相反,所以阳极的电极反应式为NaLixV3O8-xe-=NaV3O8+xLi+,NaLixV3O8中Na、O、Li元素化合价不变,则钒的化合价发生变化,失电子发生氧化反应,故C正确;
D.Li极易和水反应生成LiOH和氢气,所以电池中不可以用硫酸钠溶液作电解质溶液,故D错误;
故选D.
点评:本题考查化学电源新型电池,为高考高频点,明确原电池和电解池原理是解本题关键,难点是电极反应式的书写,知道物质的性质,题目难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列说法不正确的是( )
| A、淀粉和纤维素均为高分子化合物,两者都是工业制造酒精的原料 |
| B、CH2=CH-CH(CH3)-C≡CH经催化加氢可生成3-甲基戊烷 |
| C、等质量的甲烷、乙醇、乙醛分别充分燃烧,所耗用氧气的量依次减少 |
D、已知苹果酸的结构简式为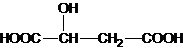 ,则该物质可发生氧化反应、酯化反应、缩聚反应,与HOOC-CH2-CH(OH)-COOH互为同分异构体 ,则该物质可发生氧化反应、酯化反应、缩聚反应,与HOOC-CH2-CH(OH)-COOH互为同分异构体 |
莽草酸可用于合成药物达菲,其结构简式如图,下列关于莽草酸的说法不正确的是( )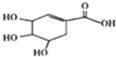

| A、分子式为C7H10O5 |
| B、1mol莽草酸与足量金属钠反应生成2molH2 |
| C、可发生加成反应、取代反应、氧化反应 |
| D、在水溶液中羧基和羟基均能电离出H+ |
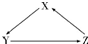 X、Y、Z为中学化学常见物质,其转化关系如下图所示(“→”表示一步转化).下列组合不正确的是( )
X、Y、Z为中学化学常见物质,其转化关系如下图所示(“→”表示一步转化).下列组合不正确的是( )| 选项 | X | Y | Z |
| A | SiO2 | H2SiO3 | Na2SiO3 |
| B | Na | Na2O2 | NaOH |
| C | H2SO3 | SO2 | H2SO4 |
| D | HClO | Cl2 | HCl |
| A、A | B、B | C、C | D、D |
化学与生产生活、环境保护密切相关.下列说法中不正确的是( )
| A、食盐既可作调味品也可作食品防腐剂 |
| B、向海水中加入净水剂明矾可以使海水淡化 |
| C、加大石油、煤炭的开采速度,增加化石燃料的供应不利于“蓝天工程”的建设 |
| D、高铁车厢材料大部分采用铝合金,因为铝合金强度大、质量轻、抗腐蚀能力强 |
下列说法正确的是( )
| A、只含一种分子的物质是纯净物,只含一种元素的物质也是纯净物 |
| B、酸的分子式中有几个氢就是几元酸 |
| C、金刚石、石墨、C60互为同素异形体 |
| D、C、N、O三种元素的第一电离能:C<N<O;电负性:C<N<O |
设NA为阿伏加德罗常数的值,N表示粒子数.下列说法正确的是( )
| A、0.1 mol苯乙烯中含有碳碳双键的数目为0.4NA |
| B、将1molCl2通入到水中,则N(HClO)+N(Cl-)+N(ClO-)=2[NA-N(Cl2)] |
| C、一定条件下,0.1 mol SO2与足量氧气反应生成SO3,转移电子数为0.2NA |
| D、电解精炼铜,当电路中通过的电子数目为0.2NA时,阳极质量减少6.4g |